这项工作的最大影响可能是为其他生物体的合成基因组中的类似策略提供基础。
2023年3月15日,哈佛医学院(HMS)的George Church实验室在《Nature》杂志上发表了一项新的研究,论文的题目是:"A swapped genetic code prevents viral infections and gene transfer."这项研究能够在利用合成生物学技术生产药物或其他有用物质时避免病毒污染带来的巨大损失。而且,该技术还可以用用于转基因生物中,能够防止转基因的逃逸及其可能带来的潜在危害。

文章称,他们已经使细菌获得了应对病毒感染的免疫能力,并获得了一种特性,能够对微生物产生生物遏制。这项工作对促进生物技术进行安全高效的应用十分有意义,并且可信的证明了使用合成基因组所开辟的可能性。
与修改活细胞中现有基因组的技术不同,合成基因组可以从零开始设计和构建。这意味着基因组变化的规模,以及由此导致的细胞功能变化的规模,不再受到现有的DNA编辑能力的限制。之前的研究中已经为模式生物大肠杆菌建立了一个功能良好的合成基因组,这个基因组的特征是改变了细菌DNA编码蛋白质的方式。
DNA决定了一个蛋白质中氨基酸的顺序和含量,而三个DNA碱基的序列,称为密码子,编码一个特定的氨基酸。密码子在整个生物学中普遍是进化保守的。为了产生一种蛋白质,DNA序列信息被复制到相应的信使RNA中。特定的转移RNA(tRNA)可以识别特定的密码子,然后将其翻译成一个特定的氨基酸,并被编码到一个正在产生的多肽链中。这段代码中存在冗余,因为大多数氨基酸可以由几个密码子编码。这使得交换相同氨基酸对应的的不同密码子成为可能,改变DNA序列,同时保持氨基酸含量。
去年秋天剑桥大学的研究人员发表了实现安全、抗病毒细菌的成果。当时使用的方法是对大肠杆菌进行基因重编程,使其从61组密码子中制造蛋白质,而不是自然发生的64组。
通过在基因组规模上改变密码子,合成的大肠杆菌基因组被设计为删除三个特定密码子。其中两个通常编码丝氨酸,另一个则指导蛋白质组装停止。负责翻译这些被删除的密码子的tRNA会在细胞中被移除或被重新用于一个新的功能。这种重新编码基因组以改变细胞DNA编码方式的过程有很多重要意义,尤其是对于细胞与病毒相互作用的过程。
病毒通常缺乏复制DNA和合成攻击宿主细胞所需的蛋白质的原料和能量。因此,它们会利用宿主细胞内的原料和能量,包括宿主细胞的tRNA库。在这种情况下,在一些tRNA被移除的合成基因组细胞中,病毒的遗传信息不能被正确翻译,使病毒与宿主不相容。
然而HMS团队意识到删除密码子是不够的,因为Nyerges和同事从环境和废水样本中鉴定出了携带自身tRNAs副本的病毒,并表明这些病毒不依赖于宿主tRNAs,可以感染被编码的细胞。为了保护工程细胞免受这类病毒的伤害,Nyerges等人开发了tRNAs,可以改变DNA编码和氨基酸含量之间的连接。
这些tRNA可以识别从合成基因组中移除的两个密码子。然而,这些tRNAs并没有像在蛋白质组装过程中那样将它们转化为亲水氨基酸丝氨酸,而是引导了疏水氨基酸亮氨酸的掺入(图a)。如果任何进入细胞的DNA序列中包含这些tRNA识别的密码子,这种变化就会产生后果。在蛋白质合成过程中,插入亮氨酸,而亮氨酸的化学性质不同于丝氨酸,这可能会改变蛋白质的结构和性质,使其失活。因此,这些细菌表达一种不同于其他自然界的“语言”,包括病毒。
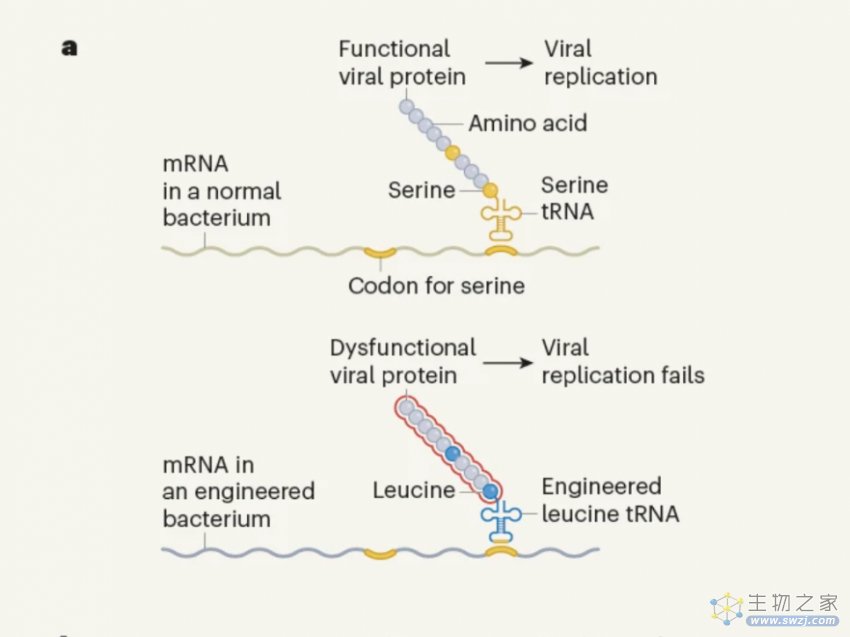
a. 作者使用了缺乏某些丝氨酸密码子的细菌,并设计了这些细菌具有识别丝氨酸密码子但携带氨基酸亮氨酸的tRNAs。病毒不能在这些细胞中复制,因为异常的亮氨酸含量会破坏病毒蛋白质
大肠杆菌合成基因组背后的团队的平行工作表明,这种方法足以防止具有自身tRNAs的特定病毒感染细胞。然而,令人惊讶的是,Nyerges等人发现,他们分离出的病毒仍然可以用修饰过的tRNAs感染和杀死细胞。对经历感染的细胞的进一步分析显示,病毒编码的tRNAs高水平产生,数量迅速超过宿主tRNAs,导致大多数病毒蛋白被正确组装和功能。
面对病毒tRNAs的这种优势,该团队决定通过吸收病毒tRNAs并产生新的版本,迫使编码从丝氨酸转向亮氨酸,从而恢复入侵的病毒。有了这些病毒衍生的替代tRNA,工程细菌可以驱动“不正确的”氨基酸并入病毒蛋白质。这些特定的病毒,以及所有其他被测试的病毒,都无法克服这种分子语言障碍,也不能感染工程细胞。
"证明交换生物体的遗传密码是可能的,这是非常具有挑战性的,也是一个很大的成就,"Nyerges说,"而且只有我们这样做的时候成功了。"
至关重要的是,作者认为,具有工程合成基因组的细菌具有前所未有的能力,可能比自然细菌种群更具有竞争优势。因此,如果微生物意外地释放到受控环境之外,可能会构成严重的挑战。
因此,作者开始通过进一步利用合成基因组的密码子变化来提高工程菌株的生物安全性。基于他们之前的一些工作,Nyerges和同事们让这些菌株对一种名为L-4,4’-biphenylalanine (BipA)的合成氨基酸“上瘾”。对细胞进行修饰,识别一个重新编码的密码子,从而将BipA并入细菌生存所需的蛋白质中,从而限制微生物在非天然分子环境中的生长(图b)。
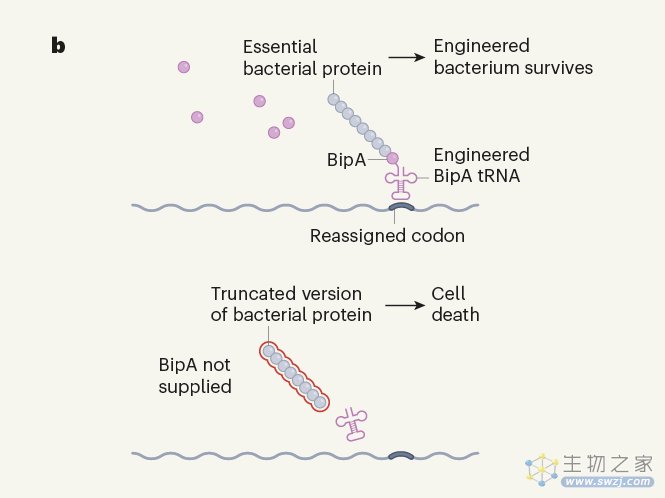
b、 作者将工程细菌中的一个密码子重新分配给携带人工氨基酸BipA的tRNA识别。一种重要细菌蛋白的mRNA含有这种重新分配的密码子,这些细菌需要BipA才能生存,这为生物防护提供了一种潜在的策略。
最后,作者证明了该编码策略可以用来防止合成DNA在可移动遗传元件序列上的传播。微生物以各种方式在细胞之间自然地交换遗传信息,包括转移被称为质粒的环状DNA分子——研究人员利用这些分子将DNA转移到细胞中。
作者创建了一套质粒,使用工程细胞的修饰密码子语言来编码在细菌中进行质粒复制所需的成分。这些质粒只能在具有合成基因组和工程tRNAs的细胞中发挥作用,这种情况显著降低了工程DNA被无意中转移到野生细菌种群的风险(图c)。
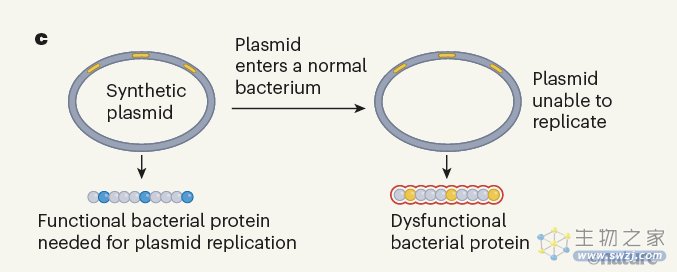
c、 作者开发了质粒,这些分子依赖于工程细菌中使用的密码子识别修饰系统。这些质粒不能在具有密码子识别标准系统的大肠杆菌中复制,从而降低了合成DNA在野外传播的风险。
作者说,尽管这项工作可能已经使一种细菌对所有病毒免疫,但仍有可能出现能够打破屏障的东西。然而,克服互换的密码子将需要病毒同时发展出几十个特定的突变。"Nyerges说:"这对自然进化来说是非常、非常不可能的。"
目前,建立一个可工作的合成基因组需要巨大的努力,目前只完成了少数基因组。我们在这方面的能力正在慢慢扩大,真核细胞的完整合成基因组预计将在未来几年完成,并致力于同样正在进行的人类合成基因组项目。随着合成基因组计划的数量、规模和雄心壮志的增加,我们研究和操纵生物学的能力也将会增加。
这项工作的最大影响可能是为其他生物体的合成基因组中的类似策略提供基础。关键的医疗产品,如疫苗和蛋白质疗法,越来越依赖于使用易受病毒感染的哺乳动物或人类细胞培养系统,这对成本和产品安全产生了重大影响。不受病毒感染问题影响的受控制、可靠的生产过程,能够最大限度地发挥这些行业的作用,对健康和福祉产生积极影响,同时确保这些过程的安全、可控,维持公信力。































