在一项新的研究中,来自美国斯坦福大学的研究人员设计了一种荧光激活细胞分选方法,从人类大脑组织中分离出不同的神经干细胞和祖细胞类型。这项研究中使用的标志物在不同的大脑区域都是保守的。该技术应有助于未来的神经发育研究,并加速开发基于神经细胞移植的治疗方案,以治疗一系列神经系统疾病。相关研究结果发表在2023年3月16日的Cell期刊上,论文标题为“Purification and characterization of human neural stem and progenitor cells”。

人脑拥有约1710亿个细胞,其中略高于一半(约860亿)是神经细胞。这860亿个神经细胞是一个多样化的细胞群体,有数百种专门的类型和功能,但都源自三个神经细胞谱系---神经元、少突胶质细胞和星形胶质细胞。这三个细胞谱系都是从神经干/祖先放射状胶质细胞(neural stem and progenitor radial glia cell)池开始的,这些神经干/祖先放射状胶质细胞在产前妊娠的第二个三个月经历了快速发育。了解这些放射状胶质细胞,它们如何分化成这三个细胞谱系,以及这三个谱系如何分化成多样化的神经细胞,将对医学研究有巨大的好处。
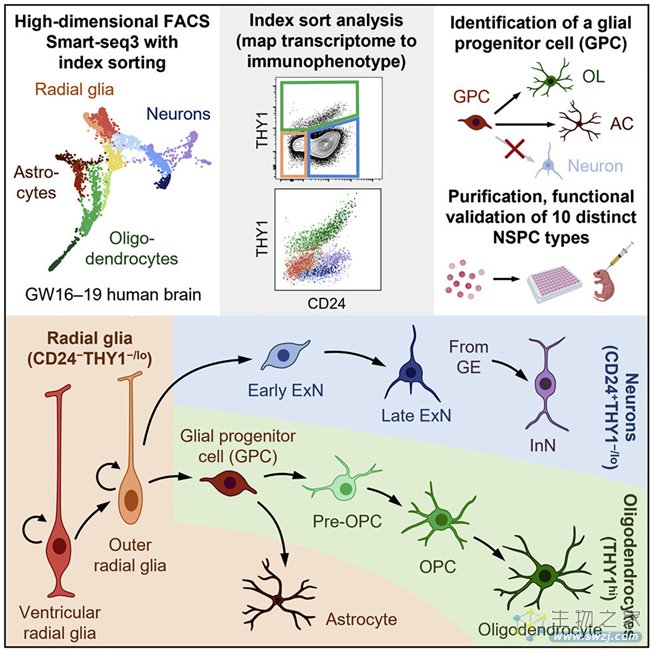
荧光激活细胞分选用于从单细胞悬浮液中根据细胞表面免疫表型分离脑组织中的细胞类型。细胞经过索引(荧光记录)并相互分离。这些分离的细胞接受单细胞RNA测序,以捕获它们各自的转录组。通过将表面标志物谱与索引和转录组相结合,这些作者如今有了每个细胞类型的图谱,可用于以后的识别。他们还测量了最初分离方案中没有使用的另外352种表面标志物的表达,这些标志物可能在未来更好地区分细胞。
索引排序数据允许每种被测序的细胞对应到它们的原始免疫表型,而且这些作者发现RNA和细胞表面蛋白的表达并不总是相关的。一些看起来相似的细胞可能有不同的功能。这种策略产生了功能相似的分选细胞群体,从而允许分离出特定的神经干细胞和祖细胞类型来进行分析。
图片来自Cell, 2023, doi:10.1016/j.cell.2023.02.017。
这些作者确定了10种神经干/祖细胞类型,并通过将它们直接移植到新生儿免疫缺陷小鼠的大脑中来确定这些细胞的行为特征。6个月后,这些细胞在整个大脑中广泛迁移和定植,并分化出所有三种主要的神经细胞谱系。通过观察单个细胞类型的扩散方式和位置,他们可以对适宜的活动位点做出一些初步推断。虽然该实验仅仅是作为一种方法的可行性测试,但是他们确实确定了一种以前没有描述过的独特的双能性胶质祖细胞(bipotent glial progenitor cell)的功能特征。
这些作者成功地进行了概念验证,并发现可以根据细胞表面标志物从发育中的大脑中分离出不同的细胞类型。如果所使用的方法可以推广到其他干细胞类型,科学家们对细胞在大脑或其他器官中发挥的特定功能、机制和层次作用的理解可能会激增。
参考资料:
Daniel Dan Liu et al. Purification and characterization of human neural stem and progenitor cells. Cell, 2023, doi:10.1016/j.cell.2023.02.017.































