我们的一生从一枚小小的受精卵开始,她/他在经历一系列细胞分裂、分化,产生各种组织、器官最终发育成胎儿。这个过程很大程度上依赖于神奇的胚胎自我组织(self-organization)潜能。这一精巧而复杂的过程是如何完成的则是一个困扰了几代发育生物学家的重要问题。
此问题之所以重要,除了人类对自身从何而来的好奇心之外,更重要的是它的答案有着重大医学意义。首先, 在分子和细胞水平上理解胚胎发育的机理将对革新检测,预防和治疗先天性遗传缺陷的临床实践提供理论支撑。其次,能指导以干细胞为基础的细胞治疗,修复疾病或衰老导致的器官损伤,例如胰岛细胞受损导致的一型糖尿病,中风或意外导致的神经损伤,抑或伴随年龄增长而出现的器官衰老 ,等等。然而,受限于伦理和胚胎获取的技术困难,生物学家对孕后2~3 周内的胚胎发育知之甚少。因此,如何在体外模拟哺乳动物尤其是人类早期胚胎发育成了近年来世界各国科学家不懈努力的方向。
2023年7月20日,位于美国德克萨斯大学西南医学中心的吴军团队在Cell杂志在线发表题为 Modeling post-implantation stages of human development into early organogenesis with stem cell-derived peri-gastruloids 的研究成果。该研究报道了一种基于3D培养可产生胚胎和胚外组织的干细胞(扩展潜能干细胞,EPSC)【1,2】,成功在体外模拟了人类早期胚胎 (2~3周)发育。

人类胚胎大约在受精后的第6天,被称为囊胚的阶段 (blastocyst) 会附着在子宫内膜上方。这个过程称为着床,通常在第8到10天完成。着床是囊胚和子宫内膜之间建立连接的过程,即囊胚的滋养层 (trophoblast)细胞和子宫内膜上皮(endometrium)之间发生直接接触。于此同时,囊胚内部的内细胞团(inner cell mass)发育成上胚层 (epiblast)和下胚层 (hypoblast)。其中上胚层最终会发育成胎儿,而下胚层将发育成卵黄囊 (yolk sac)在早期为胚胎提供养分和血液。
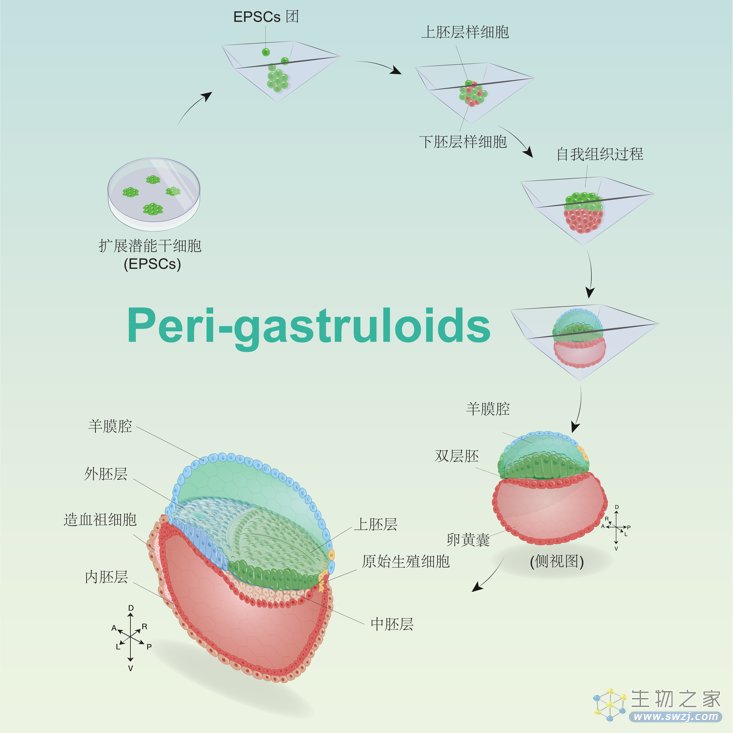
图1. 类胚胎模型(Peri-gastruloids)的产生过程。
如图1所示,为实现体外模拟早期胚胎结构,该团队利用其早先开发的一种特殊培养条件【3,4】,首先将扩展潜能干细胞变成上胚层样细胞(epiblast-like cells)和下胚层样细胞(hypoblast-like cells)。这两类细胞随后展现出惊人的自我组织行为,逐步变化为类似双层胚阶段(bilaminar disc embryo, 图2),三层胚阶段(trilaminar disc embryo, 图3),直到早期器官生成 (organogenesis, 图4)阶段的类胚胎结构。这一过程高度还原了人类胚胎在体内的发育过程。
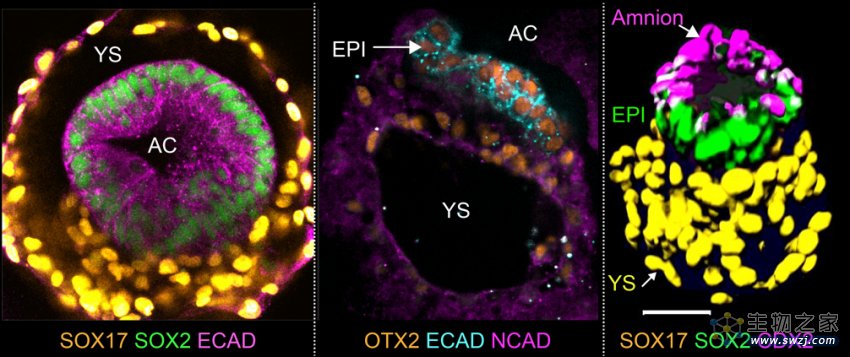
图2. 双胚层阶段(bilaminar disc)阶段。左图为俯视图,中间及右图为侧视图。
羊膜腔(amniotic cavity, AC); 蛋黄囊(yolk sac, YS); 上胚层 (epiblast, EPI). 比例尺, 50 微米。
如图2所示,在上胚层样细胞(SOX2阳性)和下胚层样细胞(SOX17阳性)首先分别产生类似羊膜腔和卵黄囊的空腔。其中羊膜腔分别由顶部的羊膜样细胞(CDX2阳性)和上胚层样细胞环绕。包括人类在内的灵长类胚胎发育过程中,羊膜细胞充当了发育信号中心的角色,由它分泌的信号分子会诱导上胚层开始原肠胚运动(gastrulation)从而产生原始的三胚层细胞,即外胚层,中胚层和内胚层。外胚层最终发育成为神经系统、皮肤等组织;中胚层发育成为心脏、血液、肌肉和骨骼等组织;内胚层则发育成为肺、肝脏、胰腺和肠道等内部器官。
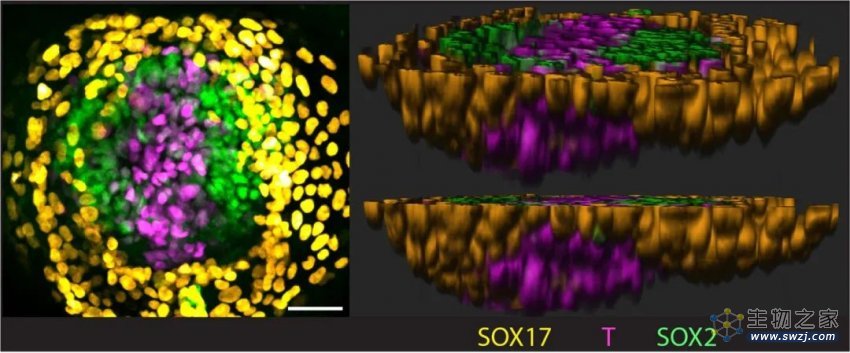
图3. 三胚层阶段(trilaminar disc)。该阶段的形态特征是原条结构(primitive streak),如图中粉色细胞所示。
左图为俯视图,右图为不同角度的侧视图。比例尺,50微米。
伴随着双胚层结构及羊膜细胞的产生,研究者继而又观察到这一类胚胎结构继续发育成三胚层结构,并伴随原条 (primitive streak) 的形成。这一结构普遍存在于哺乳动物三胚层阶段,此次为首次在体外成功模拟。这一发现也从侧面印证了羊膜细胞作为胚胎原肠胚运动信号发令枪的角色。参照人类胚胎发育,原肠运动的发生最早出现在孕后第13天左右,即CS6~7时期。接下来的问题是这一类胚胎结构是否可以继续往后发育?近期包括中国学者在内的国际上多家研究机构报道了这一领域的最新成果,模拟到原肠运动初期似乎是一个重要技术瓶颈,由此往后的发育未见报道【5-10】。而在这一最新的报道中,研究者发现他们的类胚胎模型并未止步于原肠运动初期。
胚胎发育进入第三周之后,胚胎的复杂程度将迅速增加。例如,一方面位于胚胎尾部(posterior)的上胚层处会产生一类双潜能细胞,称之为神经-中胚层前体细胞 (neuromesodermal progenitor, NMP)。它们将发育产生脊髓(spinal cord)以及副轴中胚层 (paraxial mesoderm)。脊髓的重要性不言自明。副轴中胚层在胚胎发育中也起着重要作用,它会发育成分节体(somite)并参与躯干骨骼、肌肉、真皮以及血管等的发育。另一方面,在胚胎的头部(anterior),外胚层细胞开始向神经外胚层分化,这是中枢神经系统发育的起始。在此项研究中,研究者观察到他们的胚胎模型出现了神经外胚层以及分节体的特征。为了进一步验证此胚胎模型与真实胚胎的相似性。研究者进行了单细胞RNA测序,并将之与近期由中国多家研究机构发表的人类第三周胚胎【11】以及同时期的非人灵长类(食蟹猴)胚胎【12,13】进行了单细胞水平的比较。结果发现此类胚胎与真实胚胎之间存在高度相似性。基因表达测序研究的结果进一步得到了结构分析实验的验证。
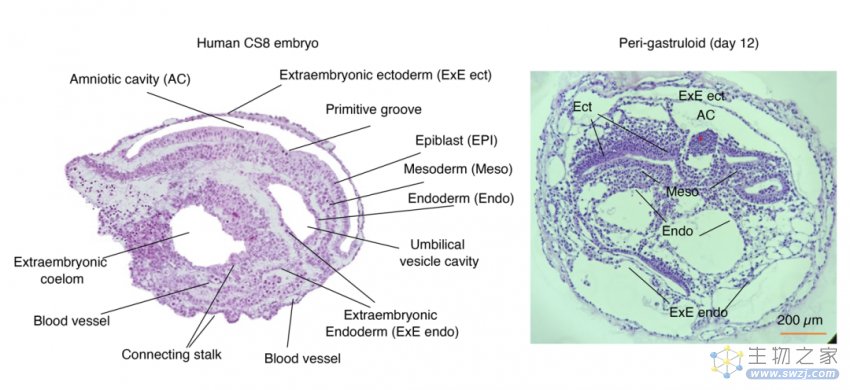
图4. 左图,为来自一颗CS8人类胚胎的组织学切片,经过H&E染色(来源于Virtual Human Embryo,切片编号为CS8_197)。
右图,来自第12天的类胚胎的组织学切片,经过H&E染色。比例尺,200 微米。
如图4所示。类胚胎在结构上展现了符合预期的高度复杂性,并与同时期的人类胚胎存在解剖结构上的相似性。到此,研究者从发育过程及最终形态上确认了这一基于干细胞的类胚胎模型与真实胚胎存在高度相似性。
综上所述,该研究描述了一种高效的方法,可以促使人类扩展潜能干细胞自组织成胚胎样结构(peri-gastruloids),其中包括胚胎(上胚层)和胚外(下胚层)组织。它重现了人类早期发育的关键阶段,如形成羊膜和蛋黄囊腔、产生双层和三层胚盘、出现原始生殖细胞 (primordial germ cell, PGC)、启动胚胎原肠运动,以及早期神经管化 (neurulation)和器官形成 (organogenesis)。单细胞RNA测序揭示了此类胚胎与人类和非人灵长类动物胚胎细胞类型之间的转录组相似性。这种胚胎样结构(peri-gastruloids),将为后续进一步在体外模拟胚胎原肠形成之后的研究提供基础,并可能有助于开发用于再生医学的人类胎儿组织。
德克萨斯大学西南医学中心吴军实验室主导了此项研究,助理讲师刘立中为该论文第一作者。该医学中心的Gary C. Hon实验室,以及宾夕法尼亚大学的Nicolas Plachta 实验室共同参与了此项研究。
吴军实验室利用种间嵌合体和干细胞模型研究基础生物学问题和开发再生医学的新应用,目前专注于衍生新型多能干细胞,识别和克服异种障碍,研究多能性的新型调节因子,并生成基于干细胞的哺乳动物胚胎模型。
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(23)00794-8
参考文献:
1. Yang, Y., Liu, B., Xu, J., Wang, J., Wu, J., Shi, C., Xu, Y., Dong, J., Wang, C., Lai, W., et al. (2017). Derivation of Pluripotent Stem Cells with In Vivo Embryonic and Extraembryonic Potency. Cell 169, 243-257 e225. 10.1016/j.cell.2017.02.005.
2. Gao, X., Nowak-Imialek, M., Chen, X., Chen, D., Herrmann, D., Ruan, D., Chen, A.C.H., Eckersley-Maslin, M.A., Ahmad, S., Lee, Y.L., et al. (2019). Establishment of porcine and human expanded potential stem cells. Nat Cell Biol 21, 687-699. 10.1038/s41556-019-0333-2.
3. Pinzon-Arteaga, C.A., Wang, Y., Wei, Y., Ribeiro Orsi, A.E., Li, L., Scatolin, G., Liu, L., Sakurai, M., Ye, J., Hao, M., et al. (2023). Bovine blastocyst-like structures derived from stem cell cultures. Cell Stem Cell 30, 611-616 e617. 10.1016/j.stem.2023.04.003.
4. Yu, L., Wei, Y., Duan, J.L., Schmitz, D.A., Sakurai, M., Wang, L., Wang, K.H., Zhao, S.H., Hon, G.C., and Wu, J. (2021). Blastocyst-like structures generated from human pluripotent stem cells. Nature 591, 620-+. 10.1038/s41586-021-03356-y.
5. Hislop, J., Alavi, A., Song, Q., Schoenberger, R., F., K.K., LeGraw, R., Velazquez, J., Mokhtari, T., Taheri, M.N., Rytel, M., et al. (2023). Modelling Human Post-Implantation Development via Extra-Embryonic Niche Engineering. bioRxiv, 2023.2006.2015.545118. 10.1101/2023.06.15.545118.
6. Pedroza, M., Gassaloglu, S.I., Dias, N., Zhong, L., Hou, T.-C.J., Kretzmer, H., Smith, Z.D., and Sozen, B. (2023). Self-patterning of human stem cells into post-implantation lineages. Nature. 10.1038/s41586-023-06354-4.
7. Weatherbee, B.A.T., Gantner, C.W., Iwamoto-Stohl, L.K., Daza, R.M., Hamazaki, N., Shendure, J., and Zernicka-Goetz, M. (2023). A model of the post-implantation human embryo derived from pluripotent stem cells. Nature. 10.1038/s41586-023-06368-y.
8. Yuan, G., Wang, J., Liu, Z., Chen, M., Zhu, P., Zhang, H., Hu, Z., Cui, Y., Yuan, Y., and Sha, J. (2023). Establishment of a novel non-integrated human pluripotent stem cell-based gastruloid model. bioRxiv, 2023.2006.2028.546720. 10.1101/2023.06.28.546720.
9. Oldak, B., Wildschutz, E., Bondarenko, V., Aguilera-Castrejon, A., Zhao, C., Tarazi, S., Comar, M.-Y., Ashouokhi, S., Lokshtanov, D., Roncato, F., et al. (2023). Transgene-Free Ex Utero Derivation of A Human Post-Implantation Embryo Model Solely from Genetically Unmodified Naïve PSCs. bioRxiv, 2023.2006.2014.544922. 10.1101/2023.06.14.544922.
10. Ai, Z., Niu, B., Yin, Y., Xiang, L., Shi, G., Duan, K., Wang, S., Hu, Y., Zhang, C., Zhang, C., et al. (2023). Dissecting peri-implantation development using cultured human embryos and embryo-like assembloids. bioRxiv, 2023.2006.2015.545180. 10.1101/2023.06.15.545180.
11. Zeng, B., Liu, Z., Lu, Y., Zhong, S., Qin, S., Huang, L., Zeng, Y., Li, Z., Dong, H., Shi, Y., et al. (2023). The single-cell and spatial transcriptional landscape of human gastrulation and early brain development. Cell Stem Cell. https://doi.org/10.1016/j.stem.2023.04.016.
12. Gong, Y., Bing, B., Nianqin, S., Baiquan, C., Honglian , S., Ting, Z., Hui, Y., Youyue, Z., Yuyu, N., Lizhong, L., et al. (2023). Ex utero monkey embryogenesis from blastocyst to early organogenesis. Cell 186, 1-19. 10.1016/j.cell.2023.04.020.
13. Zhai, J.L., Guo, J., Wan, H.F., Qi, L.Q., Liu, L.Z., Xiao, Z.Y., Yan, L., Schmitz, D.A., Xu, Y.H., Yu, D.N., et al. (2022). Primate gastrulation and early organogenesis at single-cell resolution. Nature 612, 732-+. 10.1038/s41586-022-05526-y.































