全球每年大约有 700 万人死于心脏病,随着近年来“心脏类器官”技术的发展,为探索心脏类疾病治疗带来了新机遇,但新疗法的开发仍然面临瓶颈且到目前为止,还没有整个人类心脏的生理模型。
2021年科学家开发出了具有腔室结构的心脏类器官,作为体外模型可以精准地心脏发育过程中的细胞谱系特征以及基因表达谱。
近日,奥地利科学院分子生物技术研究所 (IMBA) Sasha Mendjan 团队开发了一种心脏类器官模型,这是全球第一个能够反映心脏复杂结构的新型多腔类器官,科学家利用该多腔心脏类器官平台能够推进药物开发、毒理学研究和了解心脏发育。该研究题为“Multi-chamber cardioids unravel human heart development and cardiac defects”,发表在Cell杂志。

来源:DOI:https://doi.org/10.1016/j.cell.2023.10.030
先天性心脏病(CHD)是最常见的人类发育出生缺陷,也是胚胎和胎儿死亡的最常见原因。为了确定可能的原因和预防措施,当前需要构建涵盖人类心脏发育的所有部分的模型。对于模拟人类心脏发育的受控体外系统,必须采用体内原理来控制构建心脏时所有谱系的合并。心脏结构主要源自产生特定心肌细胞(CM)谱系的三个祖细胞群:第一心野 (FHF) ,前第二心野 (aSHF) ,后第二心野 (pSHF)。
2021 年,Mendjan实验室推出了第一个由人类诱导多能干细胞形成的室状类器官心脏模型。这些自组织的心脏类器官(或心形类器官)再现了胚胎发生早期心脏左心室的发育。作者表示,这些心脏类器官是原理验证,也是向前迈出的重要一步。大多是成年人发病时虽然影响的是左心室,左心室将含氧血液泵入全身,但先天性缺陷主要影响建立和维持循环所必需的心脏其他区域。
在这项研究中,研究人员拓展了之前的工作,建立了一个多腔室心脏类器官平台,揭示了相互作用的心室如何协调收缩以及突变、药物和环境因素如何影响人类心脏发育的特定区域。
研究人员首先从aSHF和pSHF祖细胞生成心脏类器官。首先诱导中胚层,然后使用双重 WNT 和 Nodal/Activin 等信号通路诱导分化,结果证明了在心脏类器官中,该方法可以有效且均匀地生成所有三个主要心脏祖细胞。
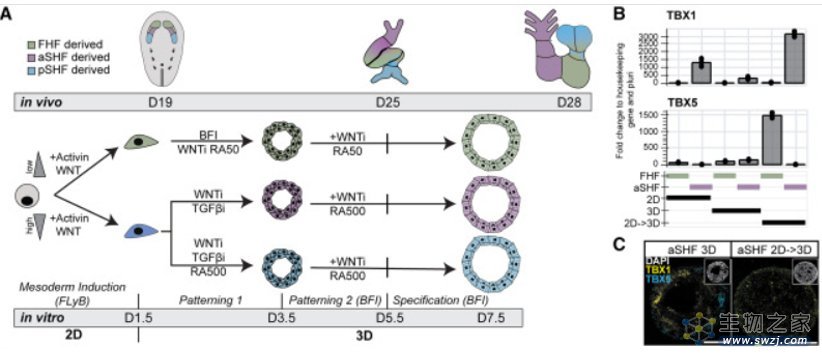
来源:DOI:https://doi.org/10.1016/j.cell.2023.10.030
FHF、aSHF 和 pSHF 在胚胎中产生几种不同的心肌细胞类型,包括心肌细胞CM 和内皮细胞EC。之前的研究表明,FHF 祖细胞产生包含 CM 和 EC 的左心室样收缩心脏类器官。按照这种方法,研究人员继续抑制 WNT 信号传导,同时用 BMP、FGF、胰岛素和 RA 处理 aSHF/pSHF 祖细胞,导致在高浓度下可重复形成包含收缩腔的心脏类器官。总之,通过应用体内类信号传导和细胞数量优化,aSHF/pSHF 祖细胞可以有效分化为心形系统内的 CM 和内皮谱系。
除了右心室之外,aSHF 祖细胞还分化为流出道,从而产生主动脉瓣、肺动脉瓣和血管结构。研究人员观察到,较高的 RA 剂量促进了 aSHF 对右心室特性的规范。作为功能验证,研究人员发现与通常不会在体内产生平滑肌细胞的 FHF 相比,流出道显示出更有效的平滑肌细胞分化倾向。
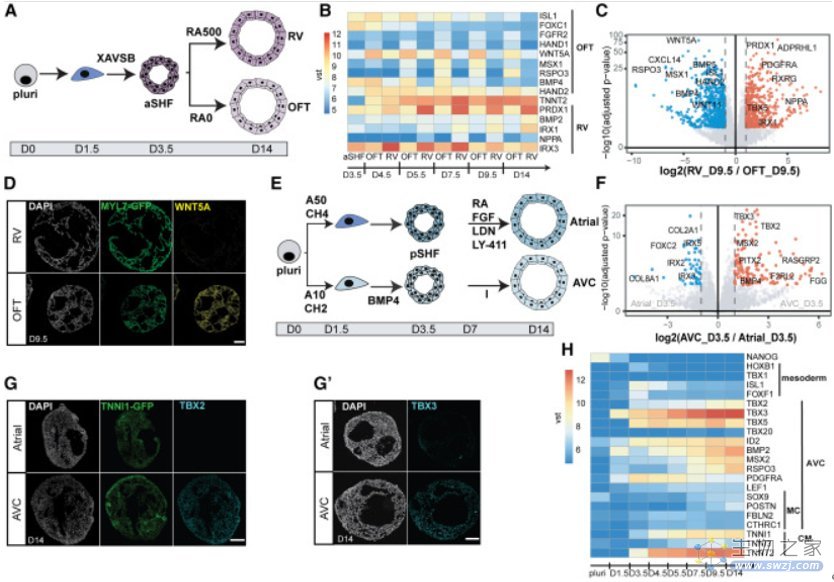
来源:DOI:https://doi.org/10.1016/j.cell.2023.10.030
在将左右心室和心房类器官一起生长后,研究人员发现电信号从心房传播到左心室,然后传播到右心室——就像动物早期胎儿心脏发育一样,这是首次在人类心脏模型及其所有心室中观察到的基本过程。
除了利用该平台研究人类发育,多腔心脏类器官还使研究人员能够研究腔室特定的缺陷。在原理验证中,研究人员建立了一个缺陷筛查平台,他们在其中研究已知的致畸剂和突变如何同时影响数百个心脏类器官。
研究人员测试了沙利度胺,这是一种众所周知的人类致畸剂,但对啮齿动物则不然,它会干扰 TBX5 功能,导致严重的心脏和四肢缺陷。研究人员使用心脏类器官平台来剖析沙利度胺在人血浆中发现的浓度范围内的作用,结果发现经过处理的样品基因表达谱和免疫染色揭示了除右心室和流出道之外的所有谱系的 TBX5 靶标下调,以及区室身份标记 NR2F2、IRX1 和 IRX4 的剂量特异性错误调节。以类似的方式,三个心脏转录因子基因的突变导致人类发育中出现的心室特异性缺陷。
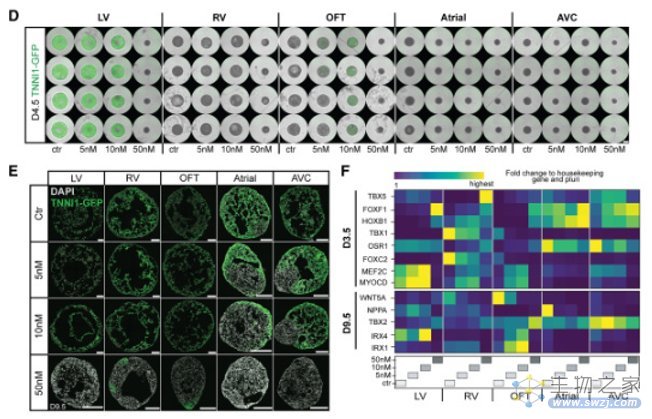
来源:DOI:https://doi.org/10.1016/j.cell.2023.10.030
总之,这些结果验证了我们可以辨别人类多室心脏平台中突变、已知致畸和致心律失常药物和治疗药物的早期发育影响,并将这些影响与在患者中观察到的心脏缺陷联系起来。因此,我们的工作对于研究从治疗开发到环境研究等背景下对人类心脏生物学的影响具有广泛的意义。我们现在有基础来研究心脏的进一步生长和再生潜力,未来多腔心脏类器官还可以应用于药理毒理学研究,从而研发出治疗心血管疾病的特异性药物。
来源:DOI:https://doi.org/10.1016/j.cell.2023.10.030































