
脊髓型肌萎缩症(SMA)是一种严重的遗传性神经肌肉疾病,是由于编码运动神经元生存蛋白(SMN)的SMN1基因纯合缺失或突变所致。SMA患者由于缺乏SMN蛋白,导致运动神经元快速死亡,肌肉功能逐步丧失,进而出现瘫痪、死亡,绝大多数1型SMA患者无法活过2周岁。
2023年3月30日,碱基编辑技术开创者刘如谦(David Liu)教授团队在 Science 期刊发表了题为:Base editing rescue of spinal muscular atrophy in cells and in mice 的研究论文。
该研究使用双AAV载体递送的腺嘌呤碱基编辑器(ABE),一次性治疗,将脊髓型肌萎缩症(SMA)小鼠模型的运动能力恢复到接近正常的水平,并显著延长了其寿命。
相比现有治疗选择,碱基编辑策略更安全、更有效,而且可以实现一次性治疗,无需重复给药。

SMA患者可能携带了不同的SMN1突变或SMN1缺失,但他们都有SMN2基因。与SMN1基因相比,SMN2基因的外显子7的第6位核苷酸出现C•G-to-T•A替代,导致其mRNA跳过外显子7,导致表达的SMN蛋白被截短并迅速降解。
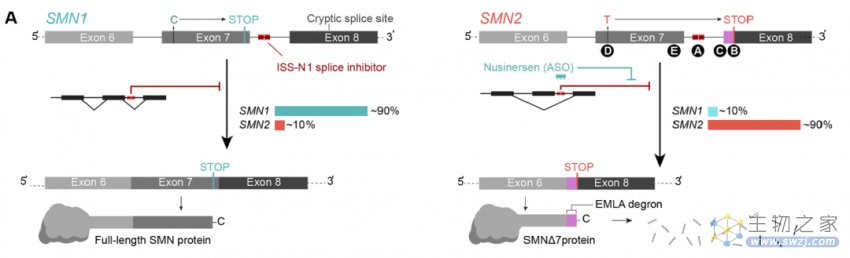
上调SMN蛋白表达可挽救SMA患者的运动功能,显著改善SMA患者预后并延长其寿命。目前共有3款SMA治疗药物,分别是渤健公司开发的反义寡核苷酸(ASO)药物Spinraza、罗氏公司开发的小分子药物Risdiplam,以及诺华公司开发的AAV基因疗法Zolgensma。
Spinraza和Risdiplam都能促进SMN2基因的外显子7在mRNA剪接中被保留,能够将SMN蛋白水平上调约2倍,但未经治疗的SMA患者脊髓中SMN蛋白仅为正常水平的不足1/6,因此,这两种药物的治疗效果有限,而且,ASO药物和小分子药物作用时间短,患者需要反复使用这种价格高昂的药物。Zolgensma是目前唯一获批的SMA基因疗法,通过静脉注射携带SMN1基因的AAV病毒载体,在体内持续表达SMN蛋白,从而一定程度上维持运动神经元生存。该疗法售价超过200万美元,一度成为全世界最贵药物。
在这项最新研究中,刘如谦教授领导的研究团队把目光聚焦于SMN2基因,尝试开发出一种适用于所有SMA患者的治疗方法。将SMN2基因中的外显子7第6位的T转换为G,从而将SMN2变为SMN1,这一策略能够将SMN蛋白恢复到正常水平,而且保留了SMN蛋白生产的自然调控机制,不用担心SMN蛋白不足导致的效果不佳,以及SMN蛋白过量表达可能导致的毒性作用。
通过结合机器学习和实验测试,刘如谦团队评估了79种针对SMN2基因不同部分的不同核酸酶编辑和碱基编辑策略,并锁定了一种能够完全恢复SMN蛋白水平、几乎没有编辑副产物,在基因组的其他地方也几乎没有脱靶效应的腺嘌呤碱基编辑器——ABE8e。
该团队最终选择了一个腺嘌呤碱基编辑器,将SMN2基因中的T•A碱基对转换为C•G对,有效地将该基因转化为SMN1基因的健康副本。这种治疗使SMN蛋白水平增加了40倍,使其恢复到健康细胞的水平。
然而,研究团队使用双AAV9将对ABE碱基编辑器递送到SMA小鼠中枢神经系统,大约43%的脊髓运动神经元被递送进碱基编辑器,在这些神经元中有87%的神经元显示出SMN2转化为SMN1。接受碱基编辑治疗或Spinraza治疗的SMA小鼠在肌肉力量、协调性和身体活动水平上与健康小鼠没有差异,且接受治疗的小鼠平均寿命比未接受治疗的小鼠长6.5倍。
研究团队还将碱基编辑疗法与Spinraza、Risdiplam和Zolgensma这三种FDA批准的SMA疗法进行了比较,结果显示,碱基编辑对SMA小鼠运动能力的改善与这三种疗法相似或更好。而将碱基编辑与Spinraza联合使用时,治疗和改善效果最明显。这表明碱基编辑可能为SMA患者提供一次性治疗,并且能够改善现有疗法效果。
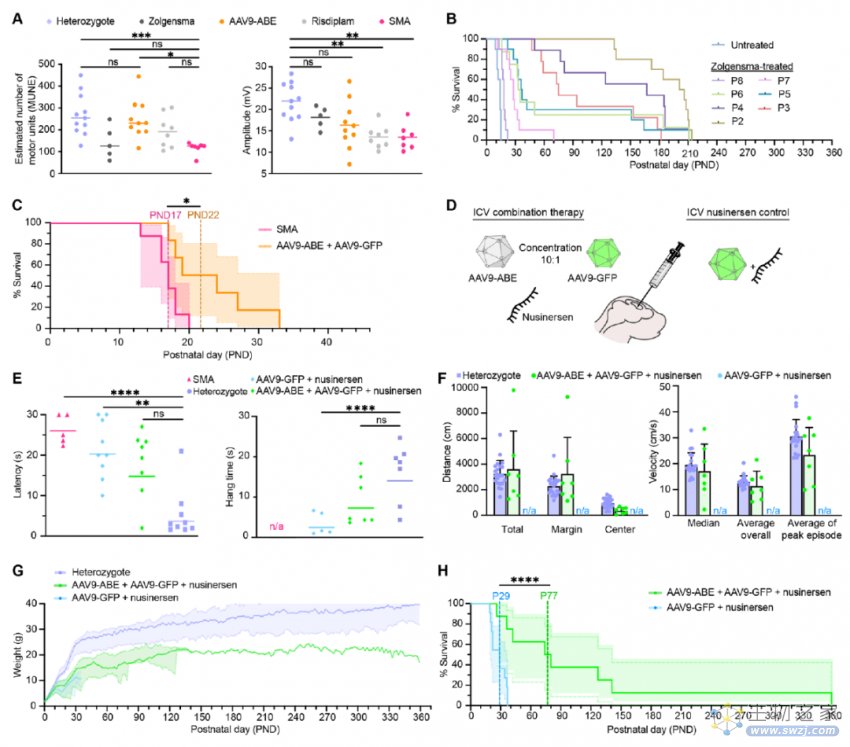
研究团队认为,碱基编辑与Spinraza联合使用带来更好的治疗效果,可能是因为Spinraza延长了SMA小鼠运动神经元能够被挽救的极短的时间窗口,让碱基编辑能够有更多时间将SMN2转化为SMN1。这个时间窗口在小鼠上只有几天,而在人类上可达几个月,因此,碱基编辑与Spinraza联合使用可能在人类身上更成功。
该研究的领导者、碱基编辑技术开创者刘如谦教授表示,这三种FDA批准的药物已经彻底改变了许多SMA患者的治疗,但精确基因编辑疗法的真正前景是,为患者带来一次治疗、终生治愈的效果。
他还表示,SMA患者可能在接受新的实验性治疗之前使用现有SMA药物,因此联合疗法是未来任何测试SMA基因编辑疗法临床试验的一个有前途的选择。此外,先导编辑(Prime Editing)技术可能会在未来进一步改善SMA治疗。虽然还有很多工作要做,但更好地了解不同的基因编辑策略对SMA的影响,是开发SMA及其他严重遗传病的一次性治疗方法的重要开始。
与此同时,刘如谦团队正在开发一种更简单的单AAV传递系统,可以减少AAV剂量并简化对SMA、早衰症等疾病的治疗。刘如谦表示,希望改进的递送系统可以为这些遗传疾病的临床试验提供一条新途径。
总的来说,该研究在SMA小鼠模型上证明,碱基编辑技术能够有效保留SMA小鼠的运动能力,并显著延长它们的寿命,更重要的是,这种治疗策略不仅能够完全恢复SMN蛋白水平,还能同时保留它们在细胞中被调控的方式,相比现有治疗选择,碱基编辑策略更安全、更有效,而且可以实现一次性治疗,无需重复给药。
论文链接:
https://www.science.org/doi/10.1126/science.adg6518































