
在发表于《通讯医学》的一项研究中,来自东京医科齿科大学(TMDU)的研究人员揭示了一项具有突破性的基因组编辑技术。这项创新技术有望治疗腓骨肌萎缩症 (CMT),这是一种影响神经的相对常见的遗传性周围神经病,目前尚无临床治疗方法。

CMT的特点是四肢远端进行性的肌无力和萎缩伴感觉障碍,每10万人中约有10-80人受到影响。最常见的CMT亚型被称为CMT1A,是由编码外周髓磷脂蛋白22(PMP22)的基因重复引起的,导致受影响个体中该蛋白的水平较高。PMP22对于形成髓磷脂结构单元非常重要,髓磷脂结构单元是一种脂肪绝缘体,允许信号从四肢快速传输到大脑并返回。
研究人员尝试使用不同的技术降低CMT1A动物模型中的PMP22,但其在人类患者中的转化一直未能成功。这可能是因为现有的动物模型不具有类似人类的PMP22基因重复。这项研究旨在解决这个问题。
“我们通过从CMT1A患者身上获取细胞并将其培养成施万细胞(制造髓磷脂的细胞)来创建细胞模型。”该研究的资深作者Hitoshi Okazawa博士说。“然后我们使用一种专门的被称为AAV载体的基因组编辑技术,来减少细胞产生的PMP22蛋白的量。”
由于PMP22水平的高低都可能导致不同类型的神经疾病(称为神经病),因此研究人员必须非常小心地减少PMP22的量。他们创建并试验了不同的AAV载体,最终选择了一种能够从基因组中删除20%至40%的PMP22基因拷贝的载体。
这足以逆转施万细胞培养物中许多与CMT相关的变化,并改善这些细胞髓鞘形成的能力,从而凸显了这种治疗方法作为该疾病临床治疗方案的潜力。
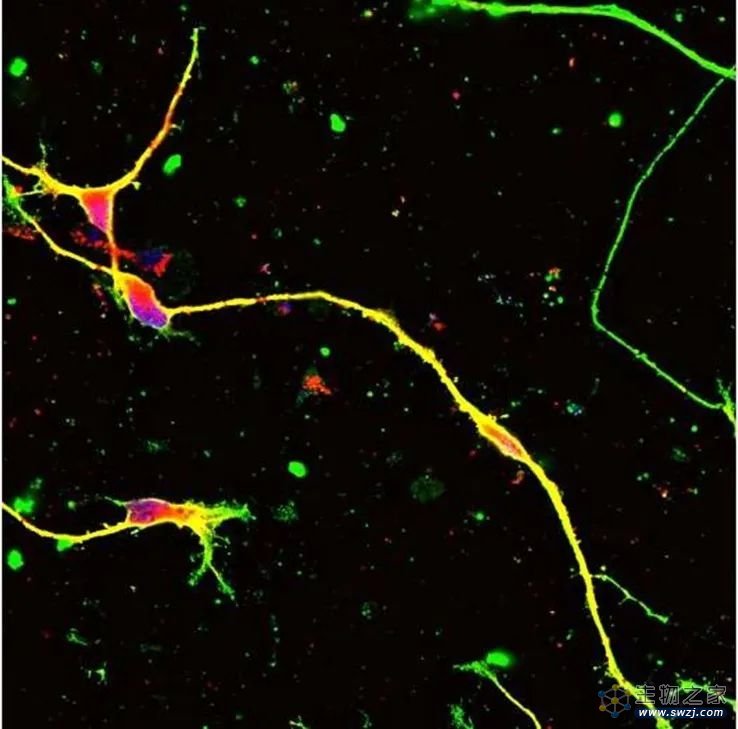
基于AAV基因治疗的基因组编辑恢复了由iPS细胞分化的人类CMT1A患者神经的髓鞘形成。图片来源:TMDU神经病理学系
“不过,在我们将这种疗法推向临床之前,还需要解决一些问题。”Okazawa博士说:“到达施万细胞的最佳注射位点目前仍然未知,并且一次或多次注射的时机可能很重要,这些都需要进一步的研究。”
研究人员对此持谨慎乐观的态度,因为类似的基于AAV的基因疗法已开始获得FDA批准用于治疗血液疾病。研究人员认为这类治疗方法对人类的应用风险较低,并且可以相对简单地转化为临床治疗。
鉴于目前除了物理治疗、职业治疗和疼痛管理外,没有其他治疗CMT的方法,开发这种PMP22基因组编辑技术是一项重要突破,有望减轻CMT患者的症状并提高生活质量。
参考文献:
Yuki Yoshioka et al, AAV-mediated editing of PMP22 rescues Charcot-Marie-Tooth disease type 1A features in patient-derived iPS Schwann cells, Communications Medicine (2023). DOI: 10.1038/s43856-023-00400-y































