
胰腺癌(Pancreatic Cancer),是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤,其中胰腺导管腺癌(PDAC)占全部胰腺癌的95%以上。近年来,胰腺癌发病率明显上升,胰腺癌早期的确诊率不高,发现时往往已是晚期,由于生存率低、预后差,胰腺癌也被称为“癌中之王”。
手术是目前治疗PDAC的唯一有效方法,但手术后仍有近90%的患者在7-9个月内(中位时间)复发,5年总生存率仅为8-10%。手术后辅助化疗能够延迟PDAC复发,但近80%的患者仍会在14个月左右复发,5年总生存率<30%。而放疗、生物制剂及靶向治疗也没有效果,此外,PDAC对免疫检查点抑制剂几乎完全不敏感(应答率<5%)。这种不敏感性部分归因于PDAC的突变率低,产生的新抗原(Neoantigens)很少,导致PDAC的抗原性弱。
然而,最近的一些研究表明,大多数PDAC实际上比之前预测的含有更多的新抗原。此外,对PDAC长期幸存者的研究表明,新抗原可能刺激PDAC中的T细胞。因此,由于大多数PDAC含有可能刺激T细胞的新抗原,递送新抗原的策略可能会诱导新抗原特异性T细胞,从而改善患者预后。
2023年5月10日,纪念斯隆凯·特琳癌症中心、BioNTech、基因泰克(罗氏子公司)的研究团队合作,在国际顶尖学术期刊 Nature 上发表了题为:Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer 的研究论文。
该研究开发了一种个性化mRNA疫苗策略——autogene cevumeran(BNT122),该疫苗通过mRNA表达PDAC患者的20种新抗原,使用LNP进行静脉注射给药。在手术切除后的PADC患者中,与化疗和免疫检查点疗法联用时,该mRNA疫苗有潜力地延缓了PDAC患者的复发。

治疗性mRNA疫苗技术促进了个性化新抗原疫苗的发展。此外,mRNA技术可以快速开发为表达多种新抗原的个性化疫苗,激活抗原呈递细胞(APC),并且可以使用已经经过临床广泛验证的脂质纳米颗粒(LNP)进行递送。
观察到PDAC的长期幸存者对肿瘤特异性新抗原产生了自发T细胞反应,但这些反应在患者之间并不相同。研究团队希望开发一款个性化mRNA,通过诱导新抗原特异性T细胞,消除肿瘤转移并延迟复发,从而为手术切除后的PDAC患者提供临床益处。
在这项1期临床试验中,研究团队结合化疗(mFOLFIRINOX方案)和免疫检查点疗法(抗PD-L1单抗),为16名手术切除后的PDAC患者注射了一种个性化mRNA疫苗——autogene cevumeran,该疫苗表达了多达20种新抗原,使用脂质纳米颗粒(LNP)递送,通过静脉注射给要。
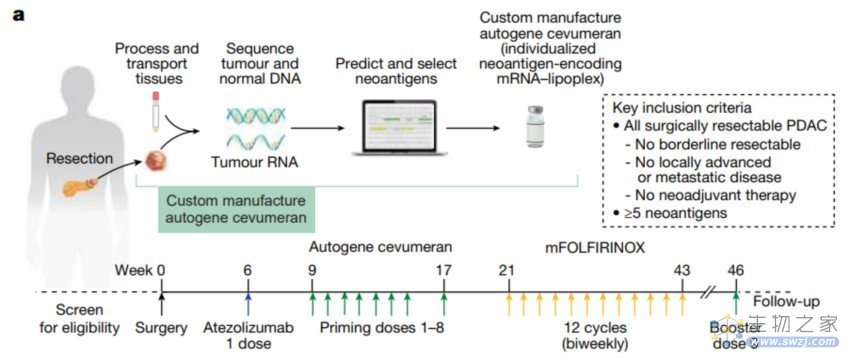
研究团队在50%的患者中观察到明显的T细胞响应,这表明该个性化mRNA疫苗可以引发增强的免疫反应。
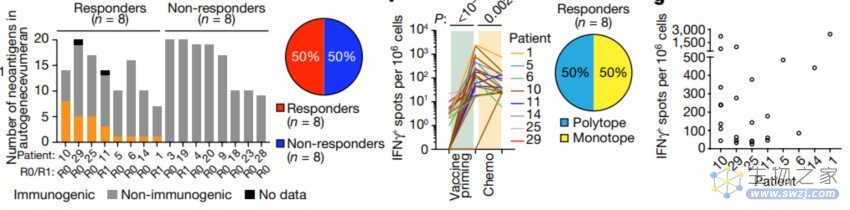
在追踪18个月后,患者免疫反应增强与复发时间延后有关,而对疫苗没有表现出响应的患者在初次评估后中位数13.4个月后出现了病情发展。
这些结果表明了个性化mRNA疫苗在治疗PDAC上的潜力,并提供了证据表明其作为一种治疗工具的一般有效性。尽管PDAC突变率低,但mRNA疫苗仍可以诱导T细胞活性对抗PDAC产生的新抗原。研究团队表示,尽管样本量有限,但这些早期结果表明有必要对这种PDAC疫苗进行更大范围的临床研究。
总的来说,该研究报告了初步临床试验证据,表明这种个性化mRNA新抗原疫苗Autogene cevumeran(BNT122)与Atezolizumab(抗PD-L1单抗)和mFOLFIRINOX(PDAC手术切除后的标准辅助化疗方案)联用,在手术切除的与延迟复发相关的PDAC患者中诱导大量T细胞活性。
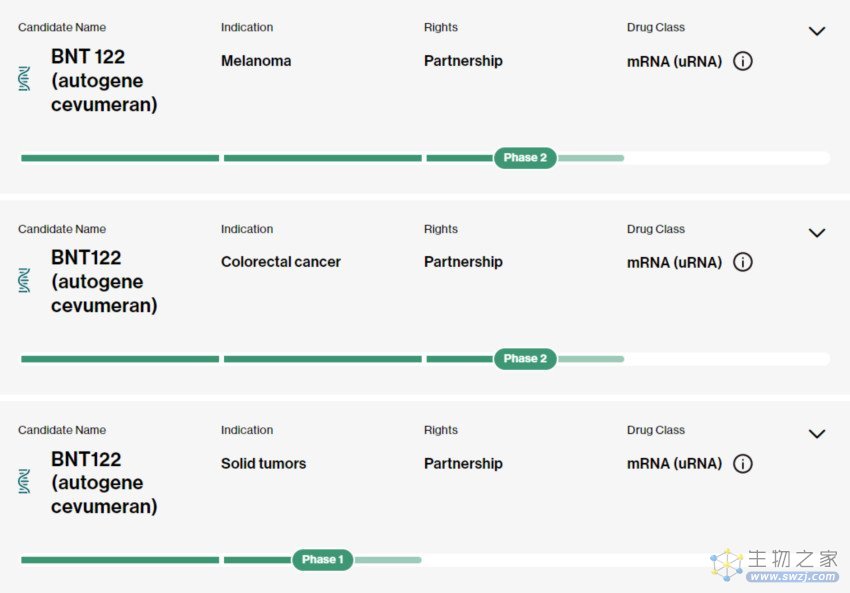
该个性化mRNA新抗原疫苗Autogene cevumeran(BNT122),由BioNTech与罗氏子公司基因泰克共同开发,目前针对黑色素瘤和结直肠癌的治疗处于2期临床试验阶段,针对实体瘤的临床试验(即该论文中的研究)即将进行2期临床试验。
论文链接:https://www.nature.com/articles/s41586-023-06063-y































