癌症、糖尿病、心血管疾病和神经退行性疾病的一个主要危险因素就是——衰老。因此,了解这衰老复杂过程的潜在机制,对于通过开发疾病新疗法来提高生活质量至关重要。寻找最有希望的治疗目标非常具有挑战性的,因为不可能用单一水平的组学数据来解释所发现的变化是衰老的原因还是衰老的结果。

那么,我们的器官究竟是如何衰老的,它们又为什么会衰老呢?
近日,斯坦福大学的研究人员在 Nature Biotechnology 期刊发表了题为:Characterizing expression changes in noncoding RNAs during aging and heterochronic parabiosis across mouse tissues 的研究论文。
该研究通过对小鼠衰老过程,以及通过异种共生实现“返老还童”小鼠的非编码RNA(ncRNA)表达图谱,鉴定了一组与衰老高度相关的miRNA,其可作为衰老的系统性调控因子,尤其是miR-29c-3p。
该研究在分子水平上对衰老有了新的认识,揭示了遗传信息的转录和翻译在老年个体上并不像在年轻个体上那样顺利,也为以RNA为靶点的药物开发提供了新方向。

表观遗传标记,例如DNA甲基化已被确定为有前途的衰老生物标志物。目前的研究,包括对老年小鼠主要器官的转录组学研究,在很大程度上缺乏覆盖整个RNA多样性的信息,例如不同类别的非编码RNA(ncRNA)。这些非编码RNA是表观遗传重编程和细胞间通讯改变的一部分,它们也被描述为衰老的标志。此外,它们还可以通过细胞外囊泡(EV)参与细胞间通讯。
众所周知,根据中心法则,DNA会转录为信使RNA(mRNA),mRNA将DNA中编码的遗传指令翻译为蛋白质,这些蛋白质反过来控制着身体的大部分新陈代谢过程。而如果mRNA分子被其他RNA所阻断,就会抑制翻译过程,从而减少蛋白质的产生。蛋白质产生受到抑制,就会影响细胞和器官的新陈代谢,最终影响整个生物体的衰老过程。
miRNA是一类非编码RNA(ncRNA),它本身不编码蛋白质,但能够靶向结合mRNA从而通过转录后基因沉默来调控基因表达。此外,miRNA可作为年龄特异性疾病生物标志物,并已被确定为衰老相关表型的调节因子。
在这项研究中,研究团队分析了小鼠衰老细胞转录组图谱(TMS)中的8类非编码RNA(ncRNA)——piRNA、lncRNA、miRNA、snoRNA、snRNA、tRNA、rRNA、scaRNA,并结合现有的单细胞和bulk mRNA数据集进行分析。涵盖了小鼠从1个月到27个月的年龄范围,以及大脑、心脏、肝脏、肺、皮肤、脾脏等16个器官和组织。
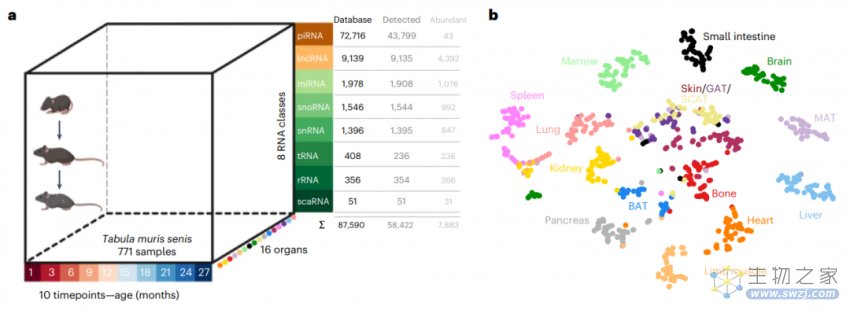
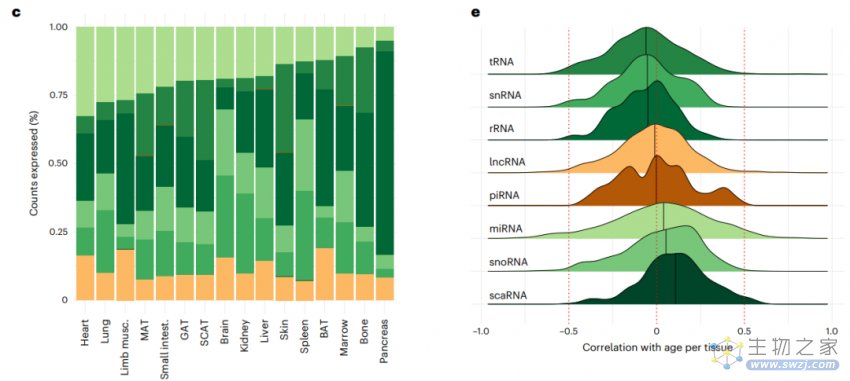
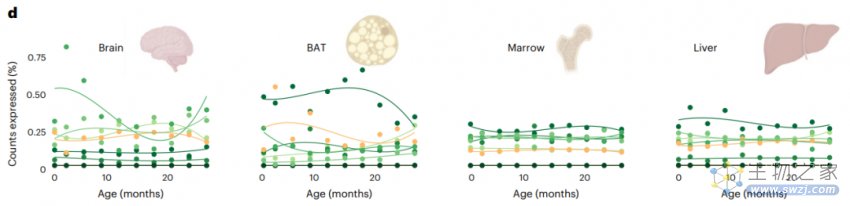
小鼠整个生命周期中的非编码RNA表达图谱
此外,研究团队还对异种共生(Heterochronic Parabiosis)实验后的组织样本进行了ncRNA测序,在实验中,一只年幼小鼠(3-4个月)和一只年老小鼠(19个月)通过手术连结共享血液循环。异种共生实验显示,年轻的血液能够促进老年小鼠恢复年轻活力,实现“返老还童”。
通过上述两项实验,研究团队探索了年龄相关的ncRNA表达变化,以及“返老还童”相关的ncRNA表达变化,以揭示ncRNA作为新的药物靶点的潜力。
研究团队将重点放在miRNA上,这是其中构成最为丰富的ncRNA群体,显示出最大的效应量,然后绘制了全局(>5个组织)和局部(≥1个组织)miRNA表达模式。根据miRNA与衰老的相关性是系统性的还是组织特异性的方式对其进行分组。尽管大多数miRNA变化是组织特异性的,但该分析还确定了8个影响全局衰老的miRNA,其中3个随着年龄的增长而减少,5个随着年龄的增长而增加。
对其中5种与衰老呈正相关的miRNA的进一步分析表明,它们的表达增加反映在转录组学变化中,这是由于参与细胞外基质(ECM)相关过程、营养感知和转录激活等调控途径的靶基因受到抑制而导致的。
而其中3种随着年龄增长而减少的miRNA的靶标在免疫系统相关过程中被富集。
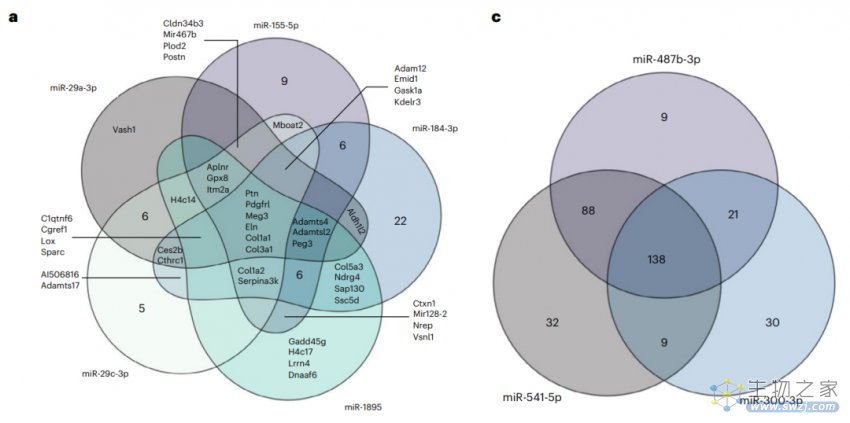
通过对异慢性异种共生实验中获得的组织样本进行的ncRNA测序显示,异种共生可以部分逆转3种与全局衰老有关miRNA的年龄相关的表达增加。
研究团队观察到,miR-29c-3p在实体器官、血浆和细胞外囊泡(EV)中与衰老相关性最大。这是一种随年龄增长而表达增加的影响全局衰老的miRNA。在异种共生实验中恢复年轻活力的小鼠中,miR-29c-3p也是最突出的miRNA,其恢复到了与年轻肝脏相似的水平。而miR-29c-3p能够靶向细胞外基质和分泌途径,已知与衰老有关。这些发现支持了miR-29c-3p通过靶向基因抑制在系统性衰老中发挥作用。
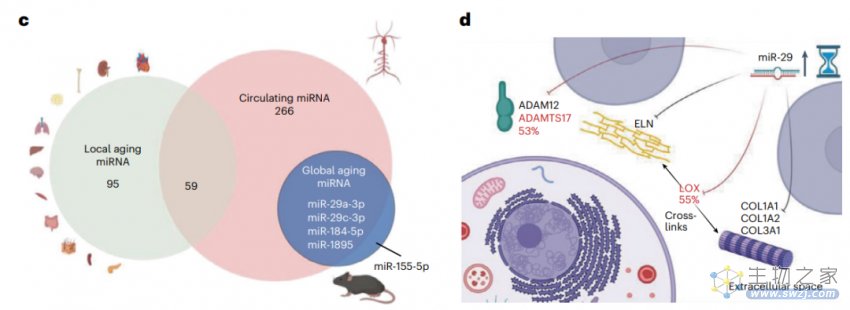
总的来说,该研究提供了衰老过程中和“返老还童”过程中的ncRNA表达图谱,并鉴定了一组衰老相关的广泛失调的miRNA,它们可能通过血浆和细胞外囊泡(EV)作为衰老的系统性调节剂发挥作用。这些实体器官健康衰老的参考数据可能支持未来基于RNA的治疗方法的发展。
研究团队表示,这些发现可以用于开发某些器官的衰老标志物还可以通过血液来观察个体的衰老过程。此外,使用最新的机器学习方法和技术,可以精确地分类不同的分子信号通路,从而获得开发创新药物的新方法,传统药物通常在蛋白质水平发挥作用,而这项研究将帮助我们把药物靶点扩展到RNA水平。
论文链接:https://www.nature.com/articles/s41587-023-01751-6































