
环状RNA(circRNA)是一类具有共价闭合环状结构的单链RNA分子非编码RNA,其在细胞中普遍存在,通常是由蛋白编码基因外显子的反向剪接形成。近年来,许多研究显示环状RNA与癌症的发生发展密切相关,通常认为,环状RNA主要通过作为miRNA的海绵、调控基因转录、编码多肽在癌症等疾病中发挥调控作用。
肿瘤发生的第一步是获得一系列基因突变来启动和维持恶性肿瘤。急性白血病的发生就是典型例子,在所有急性白血病中,大约5%-10%的患者中存在混合谱系白血病基因与超过100个已知易位伴侣基因之一发生染色体易位,产生强效致癌的基因融合,而在白血病婴儿中,这一比例超过70%。这些易位伴侣基因谱,被称为MLL重组组(MLL recombinome)。
2023年6月8日,澳大利亚弗林德斯大学的研究人员在 Cancer Cell 期刊发表了题为:Circular RNAs drive oncogenic chromosomal translocations within the MLL recombinome in leukemia 的研究论文。
该研究发现,许多人体内的特定环状RNA(circRNA)可以附着在细胞DNA上,形成环状RNA-DNA杂合体(circR Loop),进而导致DNA突变,诱导癌症发生。
这项研究提出了非编码的环状RNA的一种新型调控方式,也提出了一种源自体内的癌症发生新机制。

论文通讯作者 Simon Conn 教授表示,环境和遗传因素一直被认为是癌症的主要原因,而这项革命性发现提出了内源RNA指导的DNA损伤(ER3D),开创了一个全新的医学和分子生物学研究领域。这项研究提出了第一个例子——我们体内存在的遗传性分子有能力使我们的DNA发生突变,并从内部启动癌症。这也为在早期使用这些分子作为治疗靶点和疾病标志打开了大门。在这一阶段治愈癌症的可能性要高出很多。
研究团队对比分析了患有急性白血病的婴儿和没有任何血液疾病的婴儿的血液检测结果。结果发现,在白血病症状出现之前,一种特定的环状RNA(circRNA)在出生时的水平要高得多。某些个体细胞中circRNA分子的丰度是它们产生这些特定致癌基因的主要决定因素。
环状RNA可以在一系列细胞的不同位置与DNA结合,通过在特定位点与DNA结合,这些环状RNA会引起一系列变化,最终导致DNA锻炼。而细胞为了生存就必须去修复这些DNA,但这种修复并不总是完美的,可能会在修复过程中出现一些小的错误,例如一些碱基的错误,还可能导致大片段的更具毁灭性的突变。多个环状RNA还可能协同作用导致DNA在多个位点断裂,导致染色体易位、基因融合,将正常细胞转变为癌细胞。
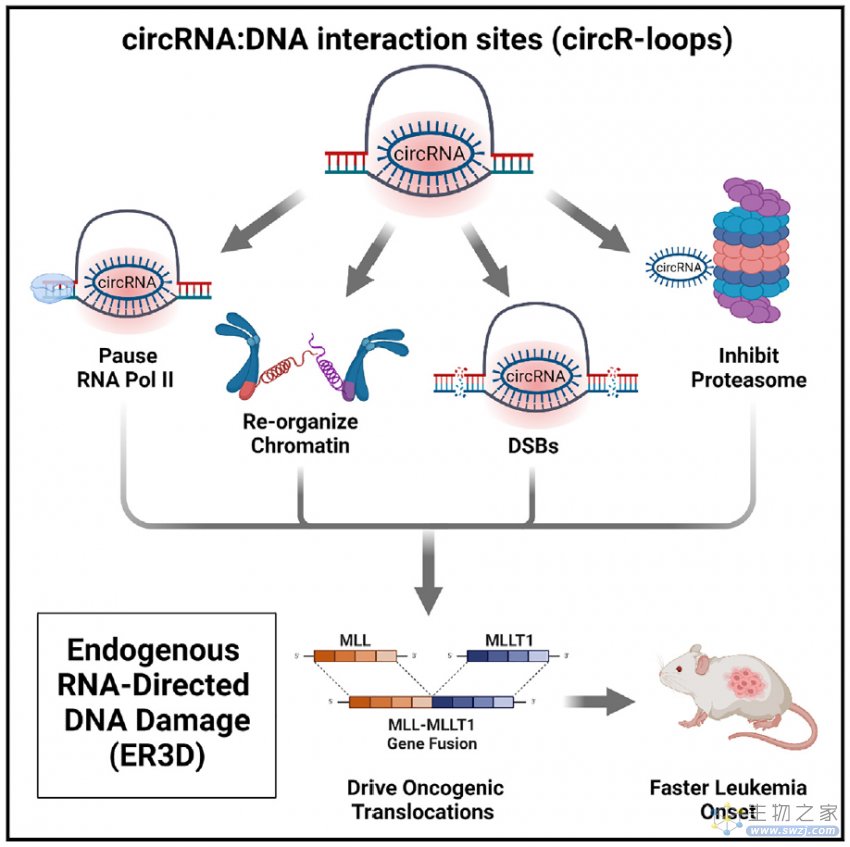
该研究发现,环状RNA在MLL重组组中富集,它们可以结合DNA,在其同源位点形成环状RNA-DNA杂合体(circR Loop)。这些circR Loop促进转录暂停、蛋白酶体抑制、染色质重组和DNA断裂。
更重要的是,在小鼠白血病异种移植模型中,过表达环状RNA会导致基因组位点的共定位,模拟MLL重组组的临床相关染色体易位的重新产生,并加速疾病发作。这些由环状RNA作用产生的基因融合发生在白血病中众所周知的突变热点区域。这些研究结果为白血病中内源性RNA致癌物导致染色体易位提供了基本见解。
研究团队还表示,ER3D不局限于白血病,还适用于其他癌症和人类疾病。研究团队正在继续研究环状RNA在癌症和其他疾病中的作用。
论文链接:https://doi.org/10.1016/j.ccell.2023.05.002































