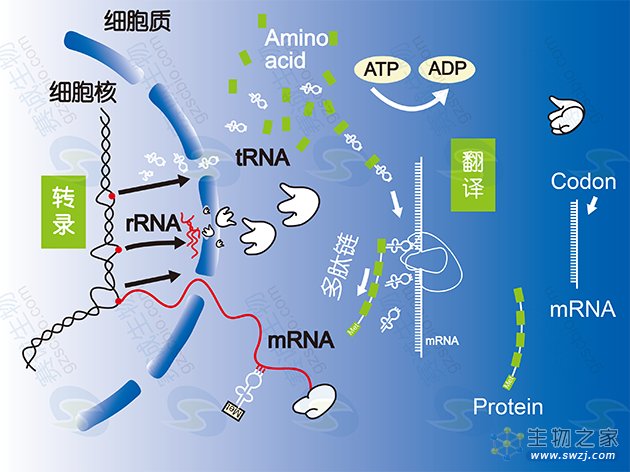
香港大学化学系、生物科学学院及生物医学科学学院的研究人员,在研究如何“读取”我们DNA中的遗传信息,以及为什么“读取”这些信息的错误往往会导致发育缺陷或癌症方面取得重大突破。研究结果发表在《科学》杂志上。

2月16日,香港大学李祥、翟元樑、黃永瀚及鲍秀丛共同通讯在《科学》(Science)在线发表题为“Menin ‘reads’ H3K79me2 mark in a nucleosomal context”的研究论文,在了解我们的DNA编码的遗传信息如何被 "读取 ",以及为什么 "读取 "这些信息的错误往往会导致发育缺陷或癌症方面取得了关键突破。
人体内的每种类型的细胞(除了一些例外)都包含完全相同的DNA序列,即基因。因此,要制造特定的细胞类型(例如干细胞、神经元),每个细胞都需要仔细地“选择”要表达的基因。这一基本过程是由组蛋白的各种修饰所调节的,以前人们认为组蛋白只是将DNA包装在细胞核中的线轴。我们现在知道,这些组蛋白修饰是染色质上的标签或标记,起着调节基因的主开关的作用——它们决定了细胞中哪组基因应该在正确的时间和正确的程度上“打开”或“关闭”。这一基本过程的失调是许多严重人类疾病(如癌症)的基础。
不同类型的组蛋白标记作为细胞信号来控制调节基因表达、DNA复制和损伤修复的各种染色质相关机制。染色质生物学的挑战之一是如何解释特定的组蛋白标记以实现其生物学功能。要回答这个问题,有必要找到“阅读者”,这是一类能够识别特定组蛋白标记并通过相应地提高或降低基因的表达来 "翻译 "它们的蛋白质。
然而,许多组蛋白标记的“阅读者”仍然未知,这限制了我们理解它们在基因调控中的作用的能力。李教授的实验室长期以来的兴趣是开发新的化学方法来识别用传统生物学方法可能难以找到的组蛋白“阅读者”。其中一种方法使用含有组蛋白标记(即组蛋白的一小段)的肽,作为识别标记的“阅读者”的“诱饵”。Li教授解释说:“成功的关键不仅是‘诱饵’,还有一个特别设计的‘钩子’,它装有一种光激活化学基团,可以在紫外线照射下捕捉‘阅读者’。”
在这项研究中,研究小组重点研究了组蛋白H3赖氨酸79 (H3K79me2)的甲基化标记。在人类细胞中,这个标记存在于积极表达的基因中。哺乳动物胚胎中H3K79me2的缺失可导致多种发育异常,包括生长受损、心脏扩张和死亡。另一方面,在儿童白血病等多种癌症中,H3K79me2被发现处于异常高的水平和错误的位置(例如促癌基因)。
尽管H3K79me2在基因调控中具有重要的生物学意义,但该标记如何“翻译”的机制尚不清楚,因为自20年前发现H3K79me2以来,还没有发现它的“阅读者”。事实上,多年来,许多实验室尝试了各种方法来寻找这些“阅读器”。
“即使使用我们以前开发的新型化学方法,识别H3K79me2‘读卡器’也是一个巨大的挑战。”有两大障碍需要克服。首先,“读取”标记可能不仅涉及标记本身,还涉及整个组蛋白,甚至组蛋白- dna复合体(称为核小体)。换句话说,通过它的“阅读器”识别H3K79me2可能需要一个原生核小体或染色质上下文。其次,“阅读器”与H3K79me2之间的相互作用可能很弱,甚至是短暂的,因此在“钓鱼”过程中很容易丢失。
“为了吸引H3K79me2的‘阅读者’,我们必须升级我们的‘诱饵’和‘钩子’,”但这并不容易。Li的实验室花了五年多的时间来开发他们的新工具。他们没有使用组蛋白的小片段,而是用化学方法合成了一个完整的核小体,该核小体具有升级的三功能“钩子”,H3K79me2作为“诱饵”。使用这项新技术,研究小组成功地识别出一种名为menin的蛋白质作为H3K79me2的“阅读器”。
为了了解menin如何“读取”H3K79me2标记,该团队采用了一种称为冷冻电子显微镜的尖端技术来可视化这种相互作用的分子细节。Li教授说:“阐明menin如何结合H3K79甲基化的细节是设计治疗与H3K79me2调控不当相关的癌症的新药的关键。”
这些开创性工作促进了我们对基因调控的基本生物学过程的理解。这些发现也为开发新的治疗药物来治疗由H3K79甲基化异常水平引起的人类疾病提供了新的机会。
参考文献
Menin “reads” H3K79me2 mark in a nucleosomal context































