儿童脑肿瘤是导致儿童死亡的主要癌种,亟需创新性的治疗方法。GPC2是一种在细胞表面的肿瘤蛋白,高表达于神经母细胞瘤等肿瘤组织中,少见于正常组织,先前的研究已发现靶向GPC2的药物以及CAR T细胞治疗在神经母细胞瘤中有巨大潜力。然而,虽然同样在细胞表面高表达GPC2,脑瘤的靶向GPC2疗法尚未得到探索。
2022年9月10日,费城儿童医院 Jessica B Foster 团队发表于 Journal for ImmunoTherapy of Cancer 题为 Development of GPC2-directed chimeric antigen receptors using mRNA for pediatric brain tumors 的文章, 通过分析GPC2在不同类型的儿童脑肿瘤中的表达情况,采用mRNA技术构建靶向GPC2的CAR T细胞并在体外、体内实验中检测其对于髓母细胞瘤以及高级别胶质瘤的杀伤作用,为靶向GPC2的CAR T细胞疗法用于儿童脑瘤患者以及GPC2相关免疫治疗的研发奠定了基础。
为了进一步明确GPC2在儿童脑瘤中的表达情况,研究人员分析了Open PBTA数据库中包含了20种中枢系统肿瘤类型、总计833例肿瘤的转录组(RNAseq)数据。分析发现多种中枢系统肿瘤都高表达GPC2,而正常组织中GPC2的TPM(TPM为转录本表达量的一种校正值,译者注)多在10以下(中位数0.43-4.65)。将表达量高于10TPM定义为“高表达”,100%的具有多层菊形团的胚胎性肿瘤(embryonal tumor with multilayered rosettes, ETMRS),95%的髓母细胞瘤,93%的其他中枢系统胚胎性肿瘤,50%的脉络膜丛腺癌,41%的不具备H3K28M的高级别胶质瘤以及40%的弥漫性中线胶质瘤均在此列。其中胚胎性肿瘤高表达GPC2的一致性最高,中位TPM超过了25,髓母细胞瘤中最高的是第4组,高级别胶质瘤中则是具有H3G35突变的。
与此同时,研究者还发现肿瘤中来源于7号染色体长臂22区体细胞突变的GPC2表达量很高,GPC2与MYCN表达量相关,GPC2在初发和复发肿瘤中的表达量相当,以及同为高级别胶质瘤,相较于含有FBS的培养基、无血清培养基中培养出的悬浮细胞系的GPC2表达量更高,并且表现出更强的“干性”(stem-like)等特征。
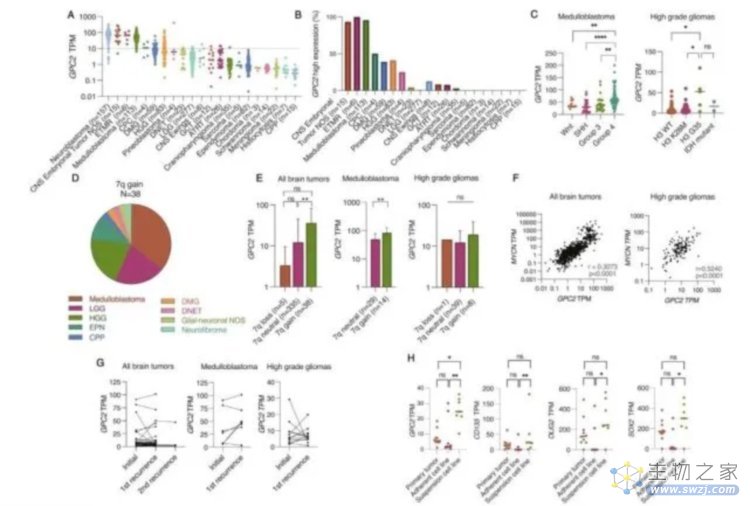
20种中枢系统肿瘤类型、总计833例肿瘤的转录组(RNAseq)数据分析结果
上述结果也在由英属哥伦比亚大学提供的脑瘤组织标本中采用免疫组化、流式以及WB等方法进行了验证。在湿实验过程中,研究者同时挑选出了分别来源于髓母细胞瘤第4组(7316-4509)以及H3G35突变的高级别胶质瘤(7316-158)的两株最高表达GPC2、且测序数据与免疫组化结果一致的脑瘤细胞系,用于后续的实验研究。
随后,研究团队将嵌合抗原受体(CAR)的scFv部分改造为D3 GPC2抗体、并使用mRNA转导及转染至人类细胞中,完成了CAR T治疗所需细胞的构建。在探索表达4种不同构造的D3 scFv(分别为D3V1、D3V2、D3V3、D3V4)的CAR T细胞作用效果的过程中,研究人员发现4种T细胞的GPC2识别能力、检查点表达情况相当。降低CAR T细胞浓度后,D3V3以及D4V4结构的CAR T 细胞在神经母细胞瘤细胞系中显现出了较强的细胞毒性,并且介导更大剂量的INFγ以及IL-2释放的能力。D3V3、D4V4 结构的靶向GPC2 CAR T细胞在髓母细胞瘤和高级别胶质瘤细胞系中也表现出了显著的选择性杀伤作用。
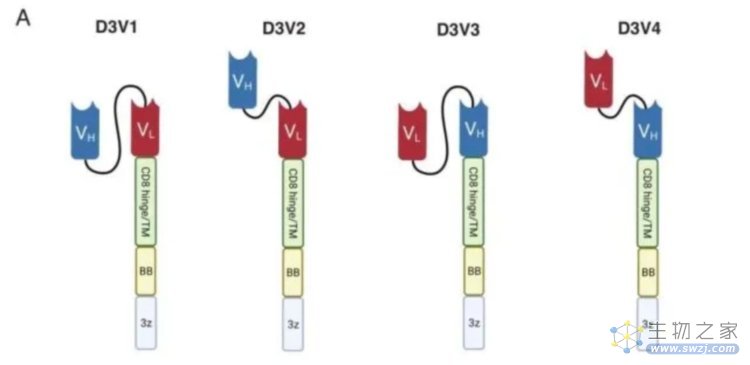
4种不同D3 scFv构造的嵌合抗原(CAR)结构示意图
最后,研究团队在髓母细胞瘤以及弥漫性中线胶质瘤的异种移植物模型中探究了D3V3和D3V4 mRNA GPC2靶向CAR T细胞在体内的作用。在完成移植物的植入后,研究者放置了一条通向肿瘤的固定管道,用于局部、针对性地定期输注治疗细胞。接受了25天的治疗后,两种CAR T细胞均可导致第4组髓母细胞瘤(7316-4509)衰退,但到第40天时仅有D3V4 CAR T细胞依旧能够发挥抗肿瘤作用。但对于第3组髓母细胞瘤(RCMB28)而言,即便是D3V4 CAR T细胞也只能短暂地抑制肿瘤生长。
此外,由于移植物抗宿主病限制了研究者观察重复剂量的CAR T 细胞在异种移植物模型中的作用效果,研究者们观察了上述CAR T 细胞对于快速生长的丘脑弥漫性中线胶质瘤(7316-3058)的作用效果。结果显示两种CAR T 细胞均显著延长了移植模型小鼠的生存期。
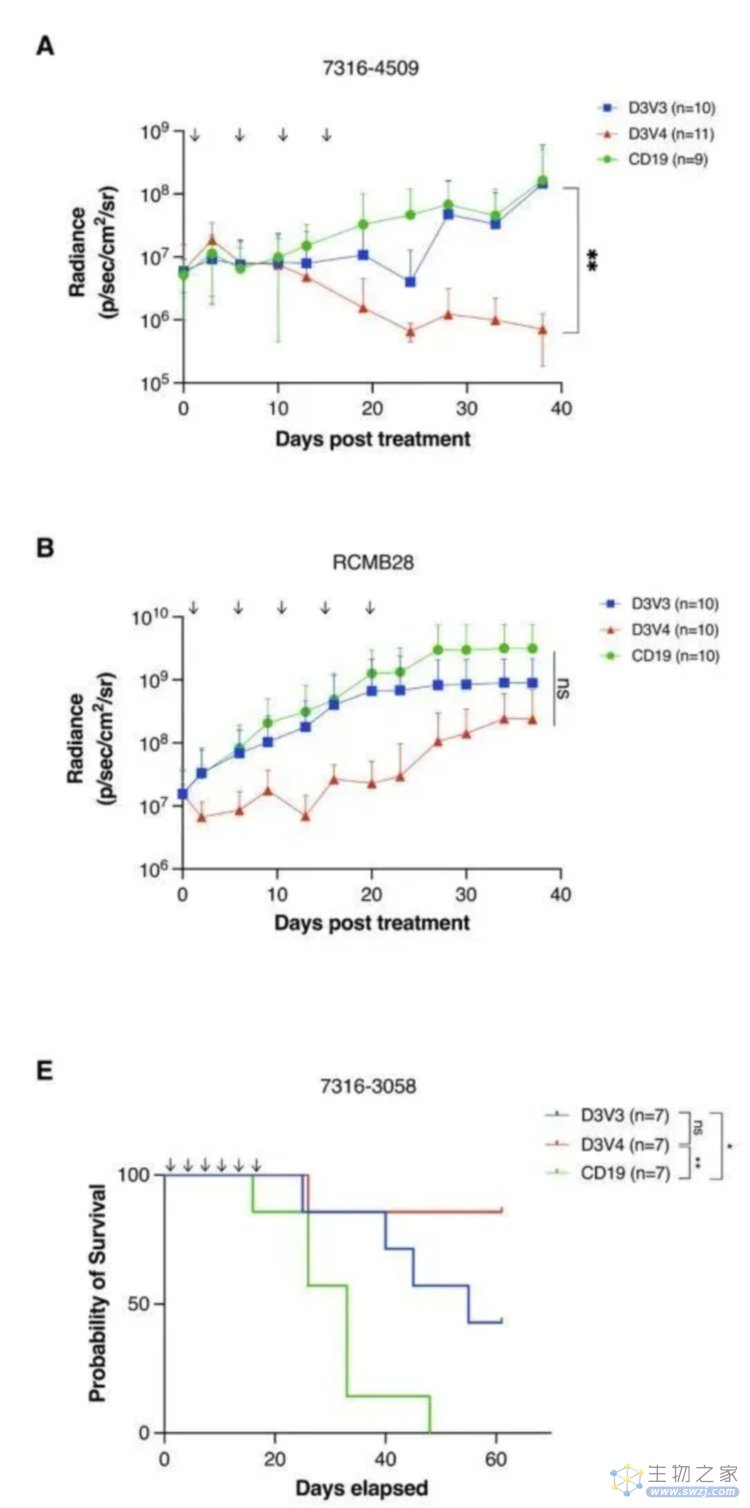
D3V3和D3V4 mRNA GPC2靶向CAR T细胞在第4组髓母细胞瘤(7316-4509)、第3组髓母细胞瘤(RCMB28)以及丘脑弥漫性中线胶质瘤(7316-3058)异种移植物模型中的作用
总之,该研究发现免疫治疗靶点GPC2在多种儿童脑肿瘤中高表达,包括恶性胚胎性肿瘤(无特殊说明的中枢神经系统胚胎肿瘤、具有多层菊形团的胚胎性肿瘤、髓母细胞瘤),以及多种高级别胶质瘤以及弥漫性中线胶质瘤。利用mRNA构造出的能够与D3 GPC2结合的有效嵌合抗原受体结构,在多种儿童脑肿瘤临床前模型中充分体现出了有依据的、概念上的有效性,为GPC2 CAR治疗相关转化打下了基础。































