1、行业回顾
1.1、市场表现:小幅跑赢沪深300指数,医药商业、中药板块表现较好
2022 年 1-12 月(统计期间为 1 月 1 日至 12 月 25 日),医药生物(申万)板块涨幅 为-11.74%,在申万 31 个一级行业(2021 年行业分类)排名 17 位,跑赢沪深 300、深证 成指、创业板指 0.89、8.52、13.81 个百分点,跑输上证综指 9.27 个百分点。分子行业来 看,医药流通、线下药店、中药板块涨幅靠前,分别上涨 7.92%、3.63%、-0.87%,疫苗、 医疗研发外包、诊断服务涨幅靠后,分别上涨-29.19%、-34.01%、-35.87%。
1.2、行业估值:相对沪深300的溢价率位于近10年低位水平
横向比较:截止 2022 年 12 月 25 日,医药生物板块 PE(TTM,整体法)均值为 24.60 倍,在申万 31 个一级行业中排名第 13 位,相对沪深 300 的溢价率为 133.74%,相对全 部 A 股(非银行)的溢价率为 40.40%。纵向比较:按日取值,医药生物板块 PE 位于自 2012 年以来后 4.60%分位数,处于历史低位水平;医药生物板块 PE 相对沪深 300、全部 A 股(非银行)的溢价率分别位于自 2012 年以来后 7.60%、19.00%的分位数。
2、创新药产业链
2.1、创新药:传统药企迎来“底部反转”,创新药企国际化可期
2.1.1、仿制药集采进度过半,部分药企逐渐走出集采阴影
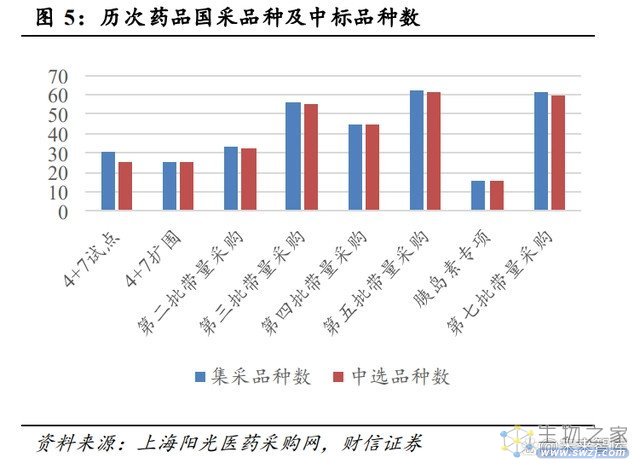
第七批国采拟中选结果公布,整体价格降幅相对温和。2022 年 7 月 12 日,第七批 国家药品集中采购在江苏南京开标。拟中选结果显示:(1)本轮集采共有 295 家企业的 488 个产品参与投标,217 家企业的 327 个产品获得拟中选资格,投标企业、投标产品的 中选比例分别为 73.56%、67.00%;(2)拟中选产品的整体平均价格降幅约为 48.00%,相 比于前五批国采 52.00%以上的降幅,本轮集采价格整体降幅略显温和;(3)部分过评家 数较多的重磅品种价格降幅较大,如奥美拉唑注射剂、奥司他韦口服常释剂型分别有 27、 12 家企业参与竞标,相比于最高申报价的拟中选价格降幅分别为 93.18%、84.70%。
仿制药集采进度过半,集采影响将边际弱化。自 2018 年以来,国家层面相继开展了 7 批药品带量采购,累计覆盖 294 个药品,涉及金额占公立医疗机构化学药和生物药年采 购金额的 35.00%。2021 年 9 月,国务院办公厅印发《“十四五”全民医疗保障规划》。《规 划》提出,到 2025 年各省(自治区、直辖市)国家和省级药品集中带量采购品种达 500 个以上。在 2022 年初的国务院政策例行吹风会上,国家医疗保障局副局长陈金甫表示, 力争到 2022 年底,通过国家组织和省际联盟采购,实现平均每个省覆盖 350 个以上的 药品品种,届时纳入集采的品种占“十四五”规划的比例将达到 70.00%。伴随着更多的 仿制药品种纳入集采,仿制药集采的影响将边际减少。
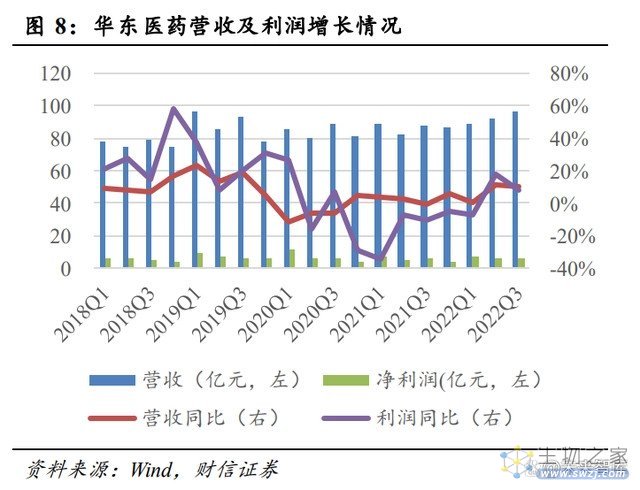
部分药企逐渐走出集采阴影。自 2021Q3 以来,受第五批药品集采等影响,恒瑞医药 业绩同比出现大幅下降。2022Q3,受益于前期基数低以及创新产品逐步放量,恒瑞医药 营收下降幅度有所收窄,仿制药集采影响趋弱。自 2022Q2 以来,受益于医药工业板块企 稳回升、工业微生物与医美等新兴业务增长良好,华东医药单季营收增速重回 10.00%以 上。可见,以恒瑞医药、华东医药为代表的传统药企正逐步走出集采影响,业绩迎来拐点。自 2022 年以来,丽珠集团、恒瑞医药、华东医药、科伦药业等企业相继推出股权激 励计划,业绩考核增速为 10.00%-20.00%,彰显企业发展信心。此外,展望 2023 年,传 统药企如京新药业、信立泰、恩华药业、华东医药等将有新产品获批上市,进一步助力 公司业绩增长。
2.1.2、医保基金支付能力增强,创新产品支付环境向好
医保基金整体运行平稳,对创新药的支付能力在增强。2022 年 1-9 月,全国医保基 金(含生育保险)总收入为 21491.18 亿元,同比增长 5.50%;全国医保基金(含生育保 险)总支出 17285.93 亿元,同比下降 0.50%,主要是去年同期支付新冠疫苗及接种费用, 本期相关支出大幅减少;全国医保基金(含生育保险)的当年结余金额达 4205.25 亿元, 结余金额已超 2020 年全年结余金额;全国医保基金(含生育保险)累计结存金额创历史 新高。
2022 年医保目录调整方案明确药品简易续约规则,利于稳定药品价格预期。2022 年 6 月 29 日,国家医疗保障局正式公布《2022 年国家基本医疗保险、工伤保险和生育保险 药品目录调整工作方案》以及《2022 年国家基本医疗保险、工伤保险和生育保险药品目 录调整申报指南》《谈判药品续约规则》《非独家药品竞价规则》。2022 年医保目录调整工 作方案明确谈判药品续约规则。谈判药品续约规则包括常规目录管理、简易续约和重新 谈判三大规则。常规目录管理:非独家产品及 2018 年谈判进入目录且连续两个协议周期 均未调整支付标准和支付范围的独家药品可以纳入常规目录管理,不再进行定期续约谈 判;简易续约:对于 2022 年 12 月 31 日到期的、协议期医保基金实际支出未超过预估值 200%、预计未来的预算增幅合理、市场环境未发生重大变化的独家产品,进行简易续约。
根据是否调整支付范围细化为两套规则,针对不调整支付范围的药品,结合比值 A(实 际支出超过预算值的比例)以及医保基金年均实际支出情况进行梯度价格下调,价格下 调幅度为 0%-25%;针对调整支付范围的药品,在不调整支付范围的药品价格降幅的基础 上,结合比值 B(未来两年因调整支付范围所致的基金支出预算增加值/本协议期基金支 出预算和基金实际支出中的高者)以及基金支出预算增加值进行梯度价格下调,价格下 调幅度为 0%-25%;重新谈判:对于不符合纳入常规目录及简易续约的独家产品,进行重 新谈判。总的来看,2022 年医保目录调整方案明确、细化了药品医保准入、续约的规则, 有利于稳定药品价格预期。

北京市医保局对创新药械试行 DRG 除外支付管理。2022 年 7 月 13 日,为激发新药 新技术创新动力,北京市医疗保障局印发《CHS-DRG 付费新药新技术除外支付管理办法 (试行)》。《管理办法》指出,对于符合申报条件的药品、医疗器械及诊疗项目,试行 DRG 除外支付管理。
其中,药械除外支付的主要条件包括:(1)创新性较高,如三年内 获批上市、三年内新增适应症、三年内新纳入医保等;(2)临床效果较传统药品/医疗器 械有较大提升;(3)对 DRG 病组支付标准有较大影响。诊疗项目除外支付的主要条件包 括:(1)公立定点医疗机构三年内在本市批准设立的新增医疗服务价格项目,非公立定 点医疗机构三年内在本市新增医疗服务价格项目;(2)临床效果较传统诊疗项目有较大 提升;(3)对 DRG 病组支付标准有较大影响。《管理办法》为能切实提升临床效用的创 新性药品、医疗器械及诊疗项目提供了较为友好的支付环境。
2022 年医保谈判延迟,预计价格降幅相对温和。2022 年 6 月 29 日,国家医疗保障 局正式公布《2022 年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案》, 从时间上看,预计 2022 年 11 月底-12 月进行医保谈判。2022 年 9 月 6 日,国家医保局公 布通过初步形式审查的 2022 年医保目录调整药品。
本次通过初步形式审查的药品数为 344 个,同比增长 26.94%。其中,通过初审的目录外西药、中成药数量分别为 184、15 个,同比增长 19.48%、150.00%。本次初审通过率约为 70.20%,高于 2021 年的 57.17%。 2022 年 12 月 6 日,国家医保局发布《关于 2022 年国家医保药品目录现场谈判延期举行 的公告》。《公告》提出,为保证现场谈判平稳有序,综合考虑新冠疫情影响和谈判工作 需要,2022 年国家医保药品目录现场谈判延期开展。具体时间确定后,将提前一周左右 通知各谈判主体。综合来看,创新药是国家医保政策重点支持的方向。在医保基金运行 平稳、医保基金累计结余不断增加、简易续约规则开始执行的情况下,预计 2022 年创新 药医保谈判价格降幅相对温和。
2.1.3、国内创新药迎来“收获期”,国际化成效日益显现
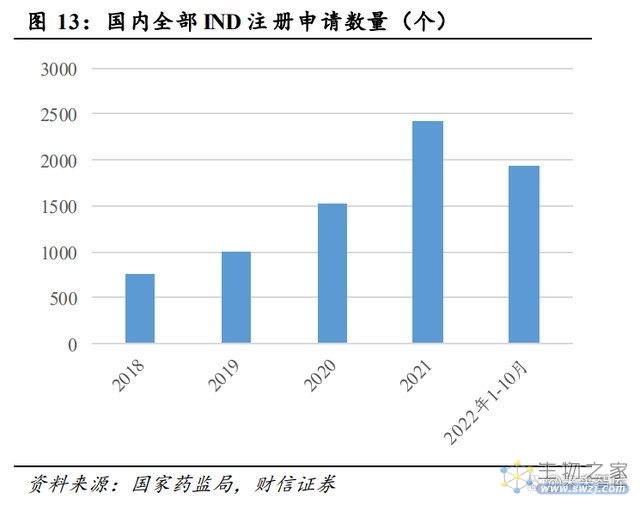
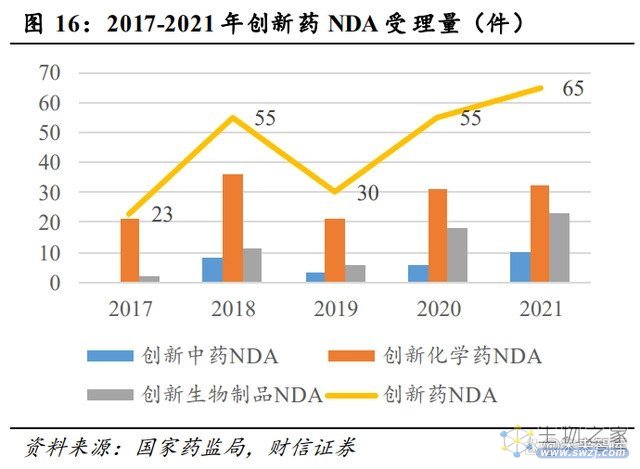
国内创新药有望迎来“收获期”。根据国家药监局的统计数据,2022 年 1-10 月,国 内 IND、NDA 数量分别为 1941、268 个,相比于 2021 年有所下降,但已接近或超过 2020 年全年数量。单看创新药情况,2017-2021 年,国内创新药 IND 数量由 483 个增长至 1821 个;国内创新药 NDA 数量由 23 个增长至 65 个。自 2021 年以来,受药审监管政策趋严、 美联储加息等因素影响,国内创新药景气度有所下降,但仍保持较高水平。
国产创新药出海路径日益清晰。2022 年 2 月 10 日,FDA 专家咨询委员会(ODAC) 未批准信迪利单抗(信达生物 PD-1)的新药上市申请,主要质疑点为:(1)仅采用中国 临床试验数据,未进行国际多中心临床研究,试验人群的多样性不足;(2)未选用一线 标准疗法作为 III 期试验(ORIENT-11)的对照组;(3)ORIENT-11 采用的主要临床终点 为无进展生存期(PFS),FDA 提倡以总生存期(OS)为临床终点。虽然信迪利单抗在 美国上市受阻,但为中国创新药出海提供了比较清晰的指引。2022 年 2 月 28 日,FDA 宣布批准传奇生物与 J&J 共同开发的西达基奥仑赛(Cilta-cel),用于治疗成人复发/或难 治性多发性骨髓瘤(R/RMM),Cilta-cel 是首款获得 FDA 批准的国产 CAR-T 细胞疗法, 也是全球第二款获批上市的 BCMA 靶向 CAR-T 疗法,为中国创新药出海注入了信心。
中国创新药国际化效果逐步显现。2022 年,中国创新药/新技术 license out 总交易金 额达 174.20 亿美元,同比增长 22.80%;交易数量达 48 项,同比增长 14.29%。从项目类 型看,创新药项目占比最高,达 71.40%,新技术及微创新(改良型)license out 交易占 比分别为 23.40%和 5.40%。从治疗领域来看,肿瘤和罕见病仍是热门交易领域,产品数 量占比分别为 35.00%和 19.00%。从单个 license out 项目规模来看,康方生物以 5 亿美元 首付款、最高 50 亿美元的总金额与 Summit 公司达成 PD-1/VEGF 双特异性抗体的海外授 权合作,为 2022 年最大的 license out 项目。在“资本寒冬”的背景下,中国创新药/新技 术总交易金额创历史最高,表明外资企业对中国药企创新能力的认可。
2022 年 10 月 12 日,百济神州公告:自主研发产品 BTK 抑制剂百悦泽®(泽布替尼胶囊)在全球 3 期 ALPINE 试验的一项终期分析中,经独立评审委员会(IRC)及研究者评估,百悦泽®对 比亿珂®(伊布替尼),取得无进展生存期(PFS)的优效性结果。百悦泽®(泽布替尼) “头对头”伊布替尼达到优效,展现“best in class”潜力,同时也反映出在部分疾病领 域,中国创新药研发水平已跻身世界前列。
2.2、CXO:行业景气度有望回升,估值修复可期
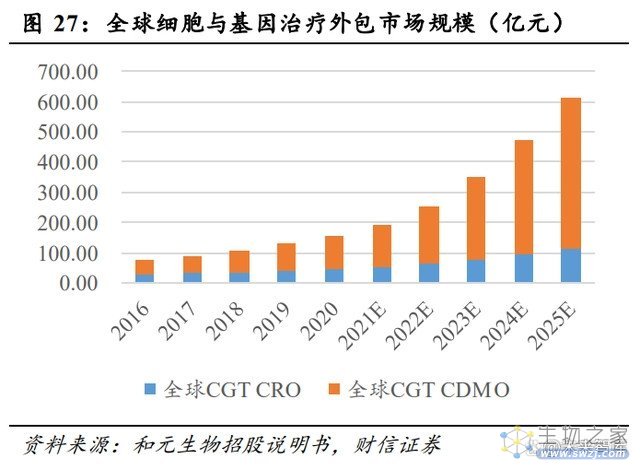
行业景气度有望回升,关注 CGT 等新兴赛道。根据动脉橙统计数据,2022 年 1-11 月,全球生物医药行业融资金额(不包括 IPO、定向增发等)约为 2158.15 亿元,同比下 降 36.20%(2022 年美元兑人民币汇率上升明显,若以恒定汇率计算,同比降幅更大), 但仍高于 2019 年全年的融资金额。从月度融资情况来看,自 2022 年 7 月以来,全球医 药生物行业月度融资金额呈现企稳趋势,同比降幅有所收窄。从医药生物科技公司二级 市场表现来看,恒生医疗保健指数、美国生物科技指数 XBI 也呈现出企稳反弹趋势。
2022 年 12 月,药明康德针对 200 多名医药生物领域的产业高管与投融资机构的调查结果显示: (1)33.30%的产业高管、51.90%的投融资机构认为 2023 年生物技术领域的投资水平会 进一步提高,整体对 2023 年产业投资持相对乐观态度;(2)超过 60.00%的产业高管与 投融资机构认为细胞和基因疗法(CGT)、RNA 疗法会成为 2023 年的投资重点。总的来看,伴随着行业政策边际回暖、美联储加息步伐放缓以及细胞与基因治疗等新兴技术快 速发展,我们认为:2023 年,CXO 行业景气度有望触底回升,细胞与基因治疗、RNA 疗法、ADC 等新兴赛道将保持高景气度。
药明生物移出 UVL 清单,行业估值修复可期。2022 年 2 月 8 日,美国商务部工业 与安全局(BIS)将 33 个总部在中国的实体列入“未经核实名单”(UVL),其中包括药 明生物在上海和无锡的两家子公司。受此消息影响,CXO 板块出现大幅下跌。根据美国 《出口管理条例》(EAR)的规定,被列入“未经核实名单”后,向名单所列的采购商、 中间收货人、最终收货人或最终用户出口、再出口或转让美国原产物项时,不得享受任 何许可例外,且必须出具“UVL 声明”。
药明生物本次受到美国出口管制的商品是生物 反应器的硬件控制器和超滤膜包,被列入清单的主要原因为:受新冠疫情影响,过去 2 年没有现场核查,美国商务部的例行程序验证未完成。2022 年 10 月 7 日,美国商务部工 业与安全局(BIS)官网显示,药明生物无锡子公司从未经核实名单(UVL)中移出。2022 年 12 月 16 日,药明生物上海药明生物技术有限公司从美国商务部的未核实清单(UVL) 中移除。本次药明生物无锡和上海工厂成功移出 UVL 清单,一方面彰显了公司运营合规 以及处置“突发事件”的能力,另一方面也将有助于缓解市场对国内 CXO 产业面临的地 缘政治风险的担忧,推动 CXO 行业估值修复。
3、中药板块
3.1、医药端、医疗端、医保端出台系列政策支持中药发展
2022 年 10 月,《二十大报告》明确提出“促进中医药传承创新发展”。相比于《十 九大报告》中的“坚持中西医并重,传承发展中医药事业”,《二十大报告》对中医药的 支持力度有所强化,更加强调创新。早在 2019 年 10 月,中共中央、国务院就印发了《关 于促进中医药传承创新发展的意见》,为中医药传承创新发展提供顶层设计。在这一顶层 文件的指引下,国家医保局、药监局、卫健委、中医药管理局等部门相继出台一系列支 持政策,涵盖医药端、医疗端、医保端等。
医药端:改革中药注册分类,健全审评审批体系,促进中药守正创新。2020 年 1 月, 国家市场监督管理总局发布的《药品注册管理办法(2020 年版)》对中药注册分类作出改 革,明确规定中药注册按照中药创新药、中药改良型新药、古代经典名方中药复方制剂、 同名同方药等进行分类,不再仅以物质基础作为划分依据,更能体现中药注册产品的创 新性等。2020 年 12 月,国家药监局印发《关于促进中药传承创新发展的实施意见》。《意 见》提出:(1)中医药研发要坚持以临床价值为导向,加强临床阶段研究和上市后研究; (2)推动古代经典名方开发,鼓励医疗机构制剂向中药新药转化;(3)构建“中医药理 论、人用经验、临床试验” 相结合的审评证据体系,对符合条件的中药实行优先审评审 批、附条件批准、特别审批。
医疗端:增强中医服务供给,鼓励运用中医技术。2021 年 6 月,国家卫健委发布《关 于进一步加强综合医院中医药工作推动中西医协同发展的意见》。《意见》明确:三级综 合医院应当全部设置中医临床科室,设立中医门诊和中医病床;有条件的综合医院特别 是有条件的三级甲等综合医院要设置中药房。此外,浙江省医保局为鼓励中医医疗机构 运用中医技术,全面实行中医医疗机构中医药服务比例与医保支付挂钩的正向激励机制。
医保端:及时纳入医保范围,中药饮片可保持 25%加成。2021 年 12 月,国家医疗 保障局、国家中医药管理局联合发布《关于医保支持中医药传承创新发展的指导意见》。 《意见》指出:及时将符合条件的中医医疗机构、中药零售药店等纳入医保定点协议管 理;按规定将符合条件的中药饮片、中成药、医疗机构中药制剂等纳入医保药品目录; 公立医疗机构销售的中药饮片可保持不超过 25%的加成比例;一般中医医疗服务项目可 继续按项目付费,中医医疗机构可暂不实行按疾病诊断相关分组(DRG)。
另外,医保端 对中药发展的支持在中成药、中药饮片集采中也得以充分体现。2022 年 4 月 8 日,广东 省药品交易中心公示广东联盟清开灵等中成药集中带量采购拟中选/备选结果。结果显示, 在拟中选/备选的代表产品中,以“最高日均费用/最高有效申报价”为基础测算,整体价 格降幅为 54.35%。其中,非独家 A 组拟中选/备选品种的平均降幅为 49.95%,非独家 B 组拟中选/备选品种的平均降幅为 84.12%,独家拟中选/备选品种的平均降幅为 17.12%, 独家品种集采价格降幅较小。
2022 年 10 月,山东等 14 省中药材集采文件(征求意见稿) 发布。本次中药饮片集采通过综合评审确定入围企业,第二轮报价确定拟中选药品,不 以降价作为唯一中选标准。其中,综合评审考虑因素包括供应能力、种植(养殖)基地、 追溯体系、生产管理能力、质量控制能力等;当第二轮报价降幅≥20%时,企业即可获 得拟中选资格。
3.2、三条中药主线:中药创新药、中药配方颗粒、品牌中药
3.2.1、中药创新药:政策成效逐渐显现,NDA数量显著增加
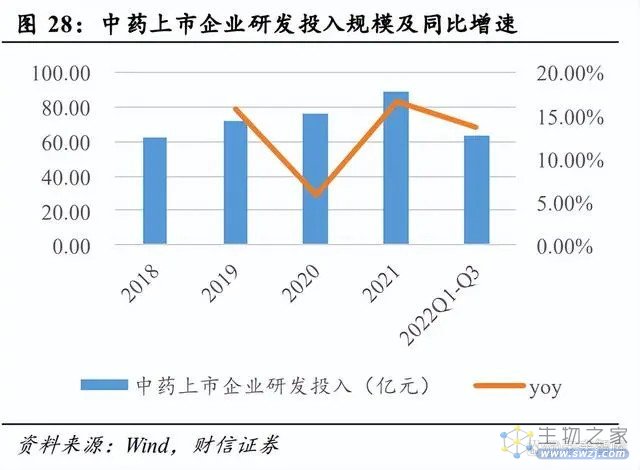
2018-2021 年,74 家中药上市企业研发投入由 62.03 亿元增长至 88.48 亿元,复合增 速为 12.57%。虽然中药上市企业的研发投入整体呈现快速增长,但投入规模明显小于化 药企业,提升空间较大。自 2019 年以来,在企业加大研发投入、中药注册分类改革、中 药审评政策优化的综合影响下,中药创新成效正逐步显现。2019-2021 年,创新中药 IND 获批数量由 14 项增长至 28 项;创新中药 NDA 获批数量由 2 项增长至 11 项,创近 5 年 之最。
3.2.2、中药配方颗粒:渗透率提升空间大,国标品种加速推进
中药配方颗粒优势明显,渗透率提升空间大。中药配方颗粒是以中药饮片为原料, 运用现代制药技术,经过提取、分离、浓缩、干燥、制粒、包装等生产工艺,加工制成 的一种统一规格、统一剂量、统一质量标准的新型配方用药。其有效成分、性味、主治、 功效和传统中药饮片基本一致,既能保留中医传统的辨证论治、灵活加减的特点,优于 中成药,又免去了病人传统煎煮的麻烦,方便有效,是中药饮片未来的发展趋势。据中 国医药工业信息中心数据统计,2021 年,我国中药配方颗粒市场规模达到 252.45 亿元, 同比增长 32.87%,呈现快速增长趋势。我国中药配方颗粒市场份额主要集中在中国中药、 红日药业、华润三九、神威药业等头部企业,竞争格局良好。当前,我国中药配方颗粒 在中药饮片中的渗透率约为 12.30%,相比于日本 60.00%左右的渗透率,仍有较大提升空 间。
国标品种加速推进,中药配方颗粒有望迎来快速增长。2001 年起,国家将中药配方颗粒纳入规范化管理,最初仅允许 6 家试点企业生产。2015 年,国家放开单味配方颗粒 的试点生产限制。2021 年 2 月,国家药监局等多部委联合发布《关于结束中药配方颗粒 试点工作的公告》,宣布于 2021 年 11 月起结束中药配方颗粒的试点工作。
《公告》明确 了中药配方颗粒的医保定位,即纳入医保支付范围的中药饮片对应的中药配方颗粒也将 纳入医保支付范围,并参照乙类管理。《公告》还进一步放开了中药配方颗粒的销售范围, 由原二级及以上中医医院(综合医院)调整为经审批或备案能够提供中医药服务的医疗 机构。自 2021 年以来,为促进中药配方颗粒的长期健康发展,国家药监局先后公布了近 300 个国家药品标准,现在各省正加快国标切换。展望 2023 年,受益于国标陆续切换完 成以及国家政策的大力支持,中药配方颗粒有望恢复快速增长。
3.2.3、品牌中药:产品提价可持续,品牌延伸打开成长空间
质量控制水平不高是我国中药发展的一大限制因素,发展高品质的品牌中药是政策 鼓励方向。2022 年出台的《“十四五”医药工业发展规划》与《“十四五”中医药发展规 划》均提出“中药质量提升工程”,明确要从中药材种植、中药生产制造、上市后研究评 价等方面系统性提升中药质量。中共中央、国务院印发的《扩大内需战略规划纲要(2022 -2035 年)》明确提出“打造中国品牌,培育和发展中华老字号和特色传统文化品牌”。
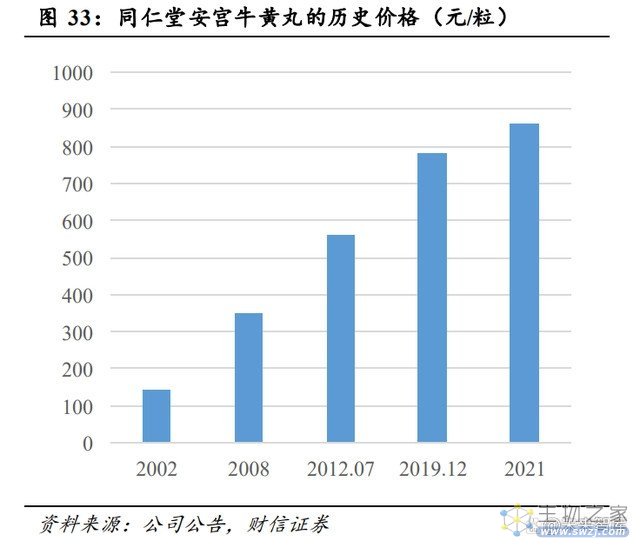
中医药是中华民族的瑰宝,拥有同仁堂、云南白药、片仔癀、九芝堂等多个中华中药老 字号品牌,品牌中药有望在国家“扩大内需战略”中的得到充分发展。从产品销售来看, 品牌中药具备形成“超级大单品”的潜质以及“持续提价”的预期。在药融云发布的 2021 年零售药店中成药销售排行榜中,多个中成药产品销售规模超 10 亿元,其中阿胶、安宫 牛黄丸、感冒灵颗粒、藿香正气口服液、健胃消食片的销售金额分别达 47.94、40.77、23.96、 16.14、15.09 亿元。通过梳理安宫牛黄丸、东阿阿胶、片仔癀等知名品牌中药的价格可知, 在过去 20 年中,前述中成药的价格呈现持续上涨的趋势。例如,同仁堂的安宫牛黄丸的 价格从 2002 年的 145 元/粒上涨至 2021 年的 860 元/粒。此外,片仔癀、云南白药等企业 借助核心产品建立的品牌优势不断拓展大健康日化业务,实现品牌价值延伸。
4、疫后复苏
4.1、零售药店:头部企业逆势扩张,疫后恢复快、持续性强
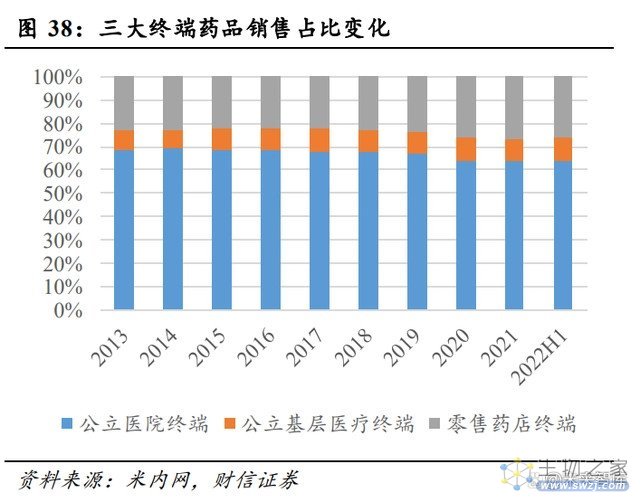
新冠疫情影响下的 2020-2022 年,公立医院终端、公立基层医疗终端的药品销售呈 现较大波动,其中两者在 2020 年均出现双位数的负增长。与之不同的是,在“四类药品” (主要指退烧、止咳、抗病毒、抗生素类药品)销售受到限制的情况下,零售药店终端 的药品销售规模实现了 3.00%-10.00%的正增长,在三大终端中的销售占比由 2019 年的 23.40%提升至 2022H1 的 26.40%,零售药店的渠道价值进一步深化。虽然新冠疫情给零 售药店企业的经营情况带来了一定扰动,但头部零售药店企业在疫情期间逆势扩张,以 老百姓为例,2020 年、2021 年、2022Q1-Q3,老百姓期内净增门店数分别达 1405、1819、 1975 家,远高于 2018 年的 1131 家、2019 年的 1264 家。
从海外国家经验来看,疫情管 控放松以后,零售药店企业的经营情况恢复明显,且增长持续性强。以美国零售药店 CVS 为例,自 2021Q1 美国逐步放松疫情管控以后,CVS 零售药房业务在 2021Q2-2022Q1 实 现了9.00%-14.00%的同比增长,并在前期基数较高的2022Q2-2022Q3实现了6.00%-7.00% 的同比增长,远高于疫情前 3.00%左右的增速水平。综合来看,伴随着国内疫情防控政 策的优化,前期受限的“四类药品”销售将恢复增长,疫情常态化下自我诊疗需求将保 持旺盛,前期逆势扩张的头部零售药店企业有望充分受益。
4.2、医疗服务:刚性医疗需求恢复速度更快,消费医疗需求恢复空间更大
肿瘤等刚性诊疗需求恢复速度更快,眼科、口腔等消费医疗需求恢复空间更大。在 新冠疫情爆发前的 2015-2019 年,全国医疗机构诊疗人次、入院人次分别以 3.19%、6.02% 的复合增速稳定增长。2020 年,受新冠疫情影响,全国医疗机构诊疗人次、入院人次分 别同比下降了 11.23%、13.47%。2021 年,受益于国内疫情防控得当,常规诊疗需求呈现 快速恢复,全国医疗机构诊疗人次、入院人次分别同比增长 9.44%、7.47%,但仅恢复至 疫前 2019 年的 97.16%、92.99%水平。
根据国家卫健委发布的《2022 年 1-6 月全国医疗 服务情况》,2022 年 1-6 月,全国医疗卫生机构总诊疗人次为 31.62 亿人次(不包含诊所、 医务室、村卫生室数据),同比增长 1.00%;医院总诊疗人次为 19.62 亿人次,同比基本 无变化。考虑到 2022 年国内疫情出现反复,我们预计 2022 年国内医疗机构的诊疗量仍 未恢复至疫情前水平。从上市民营医院的经营情况来看,在新冠疫情的影响下,通策医 疗、爱尔眼科等企业的业绩波动性加剧,且业绩增速有所放缓。
自 2022Q4 以来,国家不断优化调整疫情防控措施,减少疫情对经济发展的影响。虽然近期全国各地将陆续迎来 疫情高峰,常规诊疗恢复短期内将显著承压,但伴随着未来社会逐步回归常态,医院诊 疗需求将持续恢复。从海外各国或地区经验来看,肿瘤等刚性诊疗需求恢复更快,眼科、 口腔等消费医疗需求恢复速度相对慢一些,但恢复空间更大。
民营医院作为公立医院的重要补充,政府支持政策不变。2022 年 1 月,国家卫健委 印发《医疗机构设置规划指导原则(2021-2025 年)》。《原则》明确提出:要鼓励社会办 医,拓展社会办医空间,社会办医区域总量和空间不作规划限制;鼓励社会力量在康复、 护理等短缺专科领域举办非营利性医疗机构和医学检验室实验室等;加强社会办医的规 范化管理和质量控制,提高同质化水平;探索社会办医和公立医院开展多种形式的协作; 诊所设置不受规划布局限制,实行备案制管理。
2022 年 5 月,国务院办公厅印发《深化 医药卫生体制改革 2022 年重点工作任务》。《任务》提出,支持社会办医持续健康规范发展,支持社会办医疗机构牵头组建或参加医疗联合体。2022 年 10 月,《二十大报告》指 出,要促进优质医疗资源扩容和区域均衡布局,坚持预防为主,加强重大慢性病健康管 理,提高基层防病治病和健康管理能力;要深化以公益性为导向的公立医院改革,规范 民营医院发展。2022 年 12 月,中共中央、国务院印发《扩大内需战略规划纲要(2022 -2035 年)》。《纲要》明确指出,支持社会力量提供多层次多样化医疗服务,鼓励发展全 科医疗服务,增加专科医疗等细分服务领域有效供给。总的来看,国家支持社会办医的 政策没有变,重点鼓励社会力量参与康复、护理、基层医疗等薄弱领域,积极引导民营 医院规范发展。
4.3、血制品:国内供需缺口大,海外龙头采浆已恢复至疫情前水平
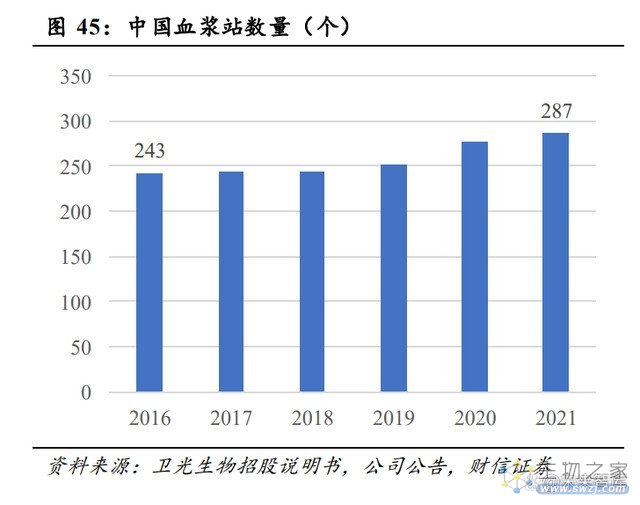
疫情防控措施优化+新设浆站数量增多,国内血浆供给有望改善。由于国内血浆监管 政策严格以及血浆具有稀缺性等,国内血浆长期处于供应紧张状态。2016-2021 年,国内 血浆站数量由 243 个增长至 287 个,复合增速为 3.38%;国内血浆采集量由 7100 吨增长 至 9390 吨,复合增速为 5.75%。过去 10 年,虽然我国血浆采集量实现了大幅增长,全 球市场份额提升至 16.00%左右,但我国仍有 60%左右的白蛋白依赖进口,血制品未能实 现自给自足。根据世界卫生组织(WHO)的建议,若要实现白蛋白自给自主,每千人血 浆采集量要达到 10L 左右(2021 年我国每千人血浆采集量约为 6.53L)。
据此测算,我国 血浆潜在需求量约为 14385 吨,相比于 2021 年 9390 吨的实际采浆量,存在 4995 吨的血 浆缺口。截止 2022 年 11 月,云南省、内蒙古省、河南省相继出台“十四五”浆站建设 规划文件,预计分别新设 17 个、6 个、7 个浆站,尚有多个省份暂未出台浆站建设规划。 据公司公告,目前,上市公司天坛生物、华兰生物、博雅生物、派林生物获批建设浆站数量分别为 23、4、1、11 个。
综合来看,“十四五”期间,国内浆站建设步伐有望加快。 此外,伴随着国内新冠疫情防控政策更加优化,存量浆站采浆不断恢复,国内血浆供给 有望出现改善。以海外血制品龙头 Grifols 为例,自 2021Q1 美国逐步放松疫情管控以来, 剔除季节、节假日因素影响,Grifols 的采浆量整体呈现企稳回升趋势。其中 2022H1,受 宏观经济环境推动、加强数字化营销、更换新型血浆设备以及提升员工经验等因素影响, 公司血浆采集量同比增加 22.00%,已恢复至疫情前采浆水平。
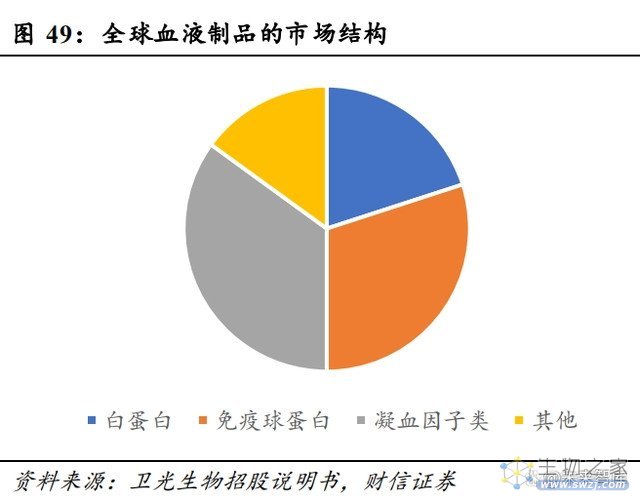
国内人均使用量低,消费需求存在翻倍空间。根据中检院、Grifols 、Wind 的数据 测算,2020 年我国血液制品的市场规模为 350-400 亿元。从结构来看,我国血液制品市场以白蛋白为主,其市场占比约为 63.00%,而全球血制品市场中白蛋白的占比约为 20.00%;我国免疫球蛋白、凝血因子类产品的市场占比分别为 31.00%、6.00%,全球免 疫球蛋白、凝血因子类产品的市场占比分别为 30.00%、35.00%。
从人均使用量来看,根 据《博雅生物 2020 年向特定对象发行 A 股股票募集说明书》中的数据,我国人血白蛋白 的人均用量为发达国家的 50.00%左右,静注人免疫球蛋白(pH4)、凝血因子Ⅷ人均使用 量分别为发达国家的 10.00%和 1.60%。比较来看,我国血制品人均使用量仍有较大提升 空间,其中免疫球蛋白、凝血因子类产品的需求提升空间更大。若假定未来我国血制品 消费结构趋近于全球水平,即白蛋白市场占比约为 20.00%,这对应我国血制品市场规模 将达到 1100-1300 亿元。
广东联盟集采(第二批)拟中选/备选结果公示,血液制品价格降幅相对温和。2022 年 5 月 27 日,广东省药品交易中心发布了《广东联盟双氯芬酸等药品集中带量采购(第 二批)拟中选/备选结果》的通知。从公示的备选结果看,静注人免疫球蛋白(50ml:2.5g)、 人免疫球蛋白(3.0ml:0.3g)、人凝血因子Ⅷ(200IU)、人纤维蛋白原(0.5g)、人血白蛋 白(50ml:10g)的平均中选价分别为 576.69、165.66、395.00、858.06、400.63 元,平均 中选价相对最高申报价的降幅分别为 37.15%、36.16%、3.79%、8.76%、33.44%。
前述 5 种血液制品的拟中选价相比于 2021 年广东联盟地区挂网采购价格的降幅均在 10%以内。 在本次广东联盟集采中,血液制品不区分 A/B 采购单,申报品规的报价低于最高有效申 报价(P0)和本企业在联盟地区的最低挂网价两者之间低值即可中选,中选企业获得联 盟地区本企业首年预采购量 100%以及增量的使用。本次广东联盟血液制品集采落地,中 选规则和中选价格降幅相对温和,压制血液制品板块表现的利空因素解除。
5、投资分析
回顾 2022 年,在地缘政治冲突、美联储加息、国内新冠疫情反复、药械集采政策等 因素影响下,医药生物板块出现了大幅波动,全年整体市场表现仅小幅跑赢沪深 300 指 数,但仍出现了新冠口服药、抗原检测、中药、医疗新基建、自我诊疗等多个结构性机 会。展望 2023 年,考虑到:(1)美联储加息步伐将放缓,以 DCF 估值为基础的创新药 资产有望迎来估值修复;(2)药明生物无锡、上海工厂相继移除“UVL”清单将有助于 缓解医药生物板块面临的地缘政治风险担忧;
(3)药械集采、医保谈判、医疗服务价格 改革、DRG 支付改革等医药政策框架更加明晰,创新药械、创新程度高与技术劳动价值 高的诊疗服务将继续享受国家政策支持;(4)国内疫情防控政策持续优化,新冠疫情影 响将逐步减弱;(5)经过 2022 年的调整,医药核心资产的估值和持仓回归均衡;我们认 为前期压制医药生物板块的因素将得以缓解,建议重视医药生物板块的配置价值,重点 把握“产业升级”与“疫后复苏”两条主线。产业升级方面,创新是医药产业发展的永 恒主题,新一轮产业政策正推动我国化学药、生物药、中药产业向高质量发展转型。
经 过多年发展,我国创新药研发在 ADC、抗体药物等部分领域已处于全球领先水平,创新 成效正逐步显现。疫后复苏方面,伴随着新型冠状病毒感染实施“乙类乙管”,前期受疫 情压制的常规诊疗需求将持续恢复,医疗机构经营、药械销售等将逐渐恢复正常。































