近40%的人会在其一生中至少经历一次晕厥(syncope)或晕厥发作(fainting spells),这种短暂的意识丧失,无论是疼痛、恐惧、炎热、换气过度还是其它原因所引起的,都占到了医院急诊室就诊患者的绝大一部分;然而,关于人们“晕厥”的确切根源机制在很大程度上研究人员并不清楚。近日,一篇发表在国际杂志Nature上题为“Vagal sensory neurons mediate the Bezold–Jarisch reflex and induce syncope”的研究报告中,来自加利福尼亚大学等机构的科学家们通过研究首次识别出了心脏和大脑之间与机体晕厥之间的特殊遗传通路。

研究人员的独特方法之一就是将心脏视为一种感觉器官,而不是长期以来认为大脑能发送信号,而心脏只是遵循指示的观点,这项研究中,研究人员运用多种方法更好的理解了心脏和大脑之间的特殊神经连接。研究者Vineet Augustine说道,我们发现,心脏也会向大脑发送信号从而改变大脑的功能,本文研究得出的信息或许更好地理解和治疗与大脑-心脏关联有关的多种精神和神经性疾病有关。我们的研究首次全面阐明了遗传定义的心脏反射,其忠实地概括了人类晕厥、在生理学、行为学和神经网络水平上的特征。
文章中,研究人员联合研究了与Bezold-Jarisch反射(BJR)相关的神经机制,BJR是一种在1867年首次被描述的心脏反射;几十年来,研究人员一直推测,以心率、血压和呼吸下降为特征的BJR或许与机体晕厥有关,但由于参与反射的神经通路目前尚不清楚,因此研究人员一直缺乏证明这一观点的信息。研究人员重点分析了称之为结神经节(nodose ganglia)的感觉簇背后的遗传学特性,其是迷走神经的一部分,能携带大脑和内脏器官(包括心脏)之间的传递信号;具体而言,迷走神经感觉神经元(VSNs,vagal sensory neurons)能将信号投射到脑干,并被认为与BJR和晕厥直接相关,在研究人员寻找新型神经通路的过程中,他们发现,能表达神经肽Y受体Y2(称之为NPY2R)的VSNs与众所周知的BJR反应密切相关。
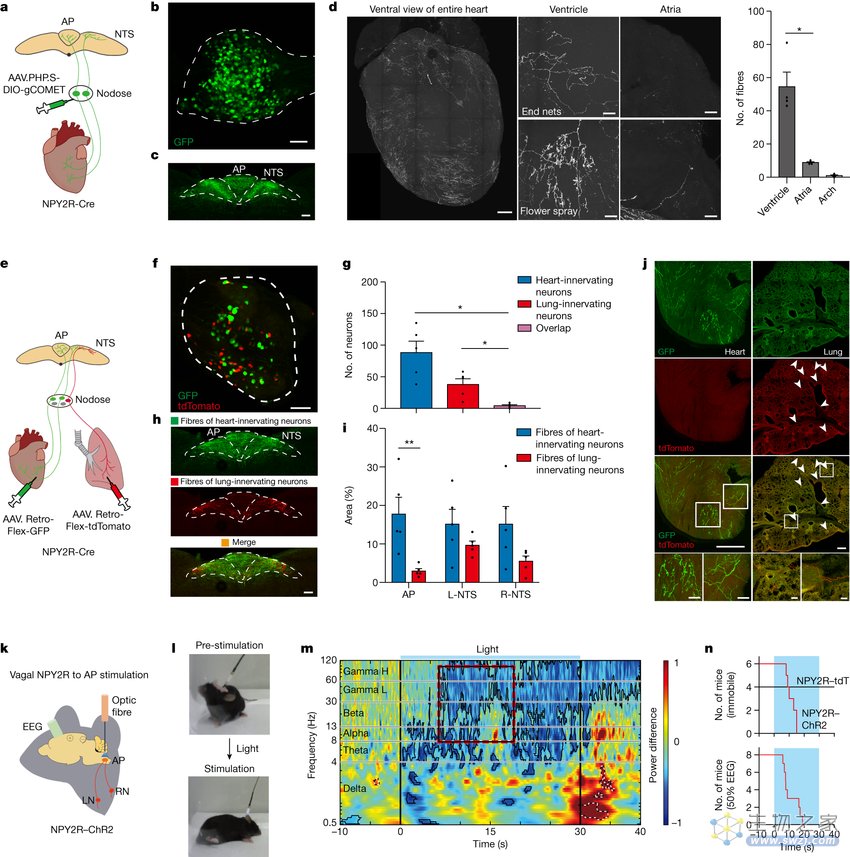
识别出新型大脑和心脏之间的关联。
图片来源:Nature (2023). DOI:10.1038/s41586-023-06680-7
随后研究人员在小鼠中研究了这一通路,他们惊讶地发现,当利用光遗传学(一种刺激并控制神经元的方法)主动出发NPY2R VSNs时,能自由活动的小鼠就会立刻晕倒。在这些事件中,研究人员记录了小鼠大脑中数千个神经元的数据,以及其心脏活动和面部特征的改变,包括瞳孔的直径和眨眼等。他们还采用多种方式来使用机器学习从而分析数据并确定所感兴趣的特征,研究者发现,一旦NPY2R神经元被激活,小鼠就会表现出快速的瞳孔扩张以及人类晕厥时的典型“翻白眼”症状,同时机体的心率、血压和呼吸率也会受到抑制。此外,研究人员还测定了流向大脑的血流量会减少。
研究者总结道,当我们看到它们的眼睛在大脑活性迅速下降的同时翻了回去时,我们大吃一惊;几秒钟后,其机体大脑的活性和运动又恢复了过来。进一步研究表明,当NPY2R VSNs从小鼠机体移除后,BJR和晕厥症状就会消失。此前的研究结果表明,晕厥是由大脑血流量减少所引起的,而这项最新研究也发现的确如此,但最新研究证据表明,大脑活动本身或许扮演着重要角色,因此,相关研究认为,新型遗传识别的VSNs机器神经通路的激活不仅与BJR有关,更重要的是还与整个动物机体的生理学、某些大脑网络甚至行为有关。
由于神经科学家们主要研究大脑,而心脏学家们主要研究心脏,所以此前研究人员很难梳理出这样的研究发现,而且许多研究都是分开进行的;研究者认为,从传统上来讲,神经科学家们认为身体只是跟着大脑走,但如今越来越多的研究都表明,机体会向大脑发送信号,随后大脑就会改变其功能。基于研究人员的最新发现,后期他们将会继续深入研究来追踪迷走神经感觉神经元被诱发开始行动背后的精确条件。研究者指出,他们还希望能更加仔细地分析在晕厥发生时机体大脑的脑血流量和神经回路,从而更好地理解这种常见但又神秘的情况。此外,研究人员还希望这一研究能作为一种模式帮助开发针对晕厥相关疾病的靶向性疗法。
综上,本文研究结果阐明了一种遗传学定义的心脏反射机制,其在生理学、行为学和神经网络水平上都概括了人类晕厥发生的主要特征。
原始出处:
Jonathan W Lovelace,Jingrui Ma,Saurabh Yadav, et al. Vagal sensory neurons mediate the Bezold–Jarisch reflex and induce syncope, Nature (2023). DOI:10.1038/s41586-023-06680-7































