端粒是一段位于染色体末端的特殊 DNA 序列,具有维持染色体稳定的作用。另一方面,它们还在细胞分裂中发挥重要作用,细胞每经历一次分裂,细胞的端粒就会随之变短,直至细胞死亡。该过程能够去除端粒非常短和基因组不稳定的细胞,并且被认为是一种防止癌症的强大屏障。然而,人们并不清楚如何才能开启这种细胞死亡程序。
近日,来自知名研究机构索尔克研究所的一组生物学家发表最新研究表明,随着人类年龄的增长与细胞分裂次数的增加,当端粒变得非常短时其将开始与线粒体发生相互作用,并且这种相互作用能够进一步触发炎症免疫反应,从而促进体内的肿瘤抑制机制,有效杀伤癌细胞。该研究论文已于 2 月 8 日发表于 Nature。

(来源:Nature)
研究表明,癌症通常是由于细胞内在遗传和表观遗传学层面发生突变所导致,这种突变能够使细胞避开由端粒所控制的增殖上限从而实现永生。
在此之前,研究人员已经发现,当端粒缩短到无法再保护染色体免受损坏的程度时,细胞就会陷入“危机”状态,其将可能通过自噬机制被清除。而在最新研究中,研究团队试图了解在端粒极短的情况下,自噬依赖性细胞死亡程序是如何被激活的。
通过对人类成纤维细胞进行基因筛选,科学家们发现了相互依赖的免疫感应和炎症信号通路,其对于处在“危机”状态的细胞死亡至关重要。具体而言,只有极短端粒发出的特定 RNA 分子(TERRA)能够在线粒体外表面以独特的方式激活先天免疫传感器 Z-DNA 结合蛋白1(ZBP1)和线粒体抗病毒信号蛋白(MAVS)。该过程中,危机相关亚型 ZBP1 的 mRNA 水平上升,且依赖于 MAVS 的干扰素 IFN 信号也有所增强,这些证据表明上述免疫传感器在人体中引发了一系列炎症免疫反应。
总体而言,该研究揭示了一种由端粒介导的肿瘤抑制机制,即功能失调的端粒能够通过线粒体 TERRA-ZBP1 复合物激活先天免疫反应,从而消除即将转化为肿瘤的细胞。
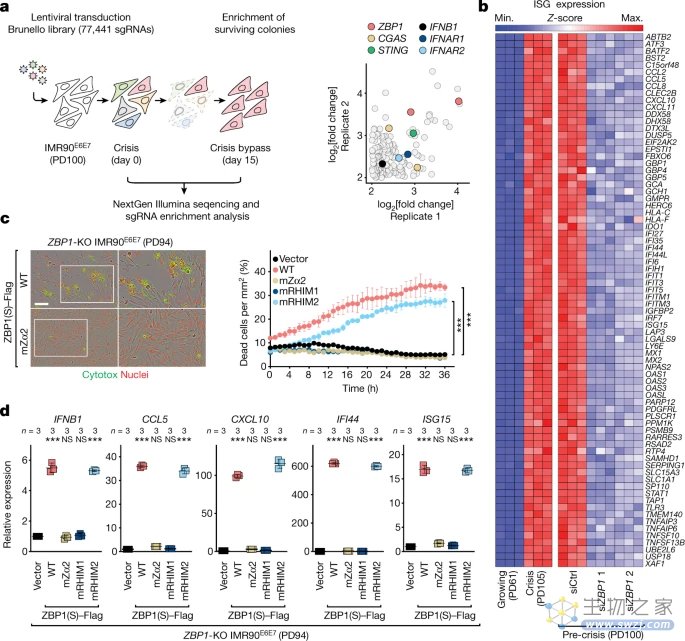
▲图丨ZBP1 在“危机”期间介导先天免疫反应(来源:Nature)
该项研究证明了存在于端粒、线粒体和炎症之间的重要联系。“我们对于端粒与线粒体之间的作用感到十分兴奋,”该研究的通讯作者之一、来自索尔克研究所的分子与细胞生物学教授 Jan Karlseder 表示,“它们能够在生物控制过程中协同发挥作用,从而启动相关通路以消灭可能发生癌变的细胞。”
长期以来,众多科学家一直在研究端粒、线粒体和炎症通路在衰老过程中所产生的变化。然而,他们此前并注意到这些变化可能将在预防癌症方面发挥作用,因为这些要素通常被单独研究,而非结合起来看待。
该研究的另一通讯作者、索尔克研究所的 Audrey Geisel 生物医学科学主席 Gerald Shadel 表示,“这可能是第一项将所有这些衰老特征联系起来的研究。当前研究结果表明,极短的端粒会向线粒体发送 RNA 以引发炎症,在此之后,我们需要更深入地了解存在于端粒和线粒体之间的复杂作用,这可能会在未来促进新型癌症疗法的发展。”
参考资料:
1.https://doi.org/10.1038/s41586-023-05710-8
2.https://www.salk.edu/news-release/telomeres-mitochondria-and-inflammation-oh-my-three-hallmarks-of-aging-work-together-to-prevent-cancer/































