癌症是全球公共健康的主要挑战之一。2020年,全球新发癌症约有1,923万例,其中,中国有457万例。各类实体瘤癌症发病率处各癌症种类前列,尤其在中国,新发病例数前五的癌症均为实体瘤,占总新发癌症数的58.7%。
虽然在过去十几年间,针对实体瘤的治疗方案在逐步改进,但现有疗法的适应症覆盖面、应答率、有效性以及副作用等各方面,远没有达到可以治疗所有患者的程度。
举例说明:传统的化疗方案虽然适应症覆盖面广,但是副作用极大,治疗精确度低;而抗体类药物靶向治疗,虽可提高治疗的精确度,与化疗相比副作用降低,但依然会有大量病人在治疗后期因无法耐受副作用,或者因肿瘤出现耐药性而停药;免疫疗法,例如PD-1、PD-L1抑制剂,有效性强、副作用小、发展前景广阔,然而却尚未实现高应答率。有一些患者,即使肿瘤出现了PD-1、PD-L1的高表达,也无法响应药物。
为了解决这些未被满足的医疗需求、克服现有疗法的缺点,对于新型疗法的研究与开发从未停歇。溶瘤病毒疗法有望达到高疗效、低副作用的效果;并且与其他疗法联用可以提高应答率,是潜在优良治疗方案。溶瘤病毒领域的生命科技公司有望成为独角兽。
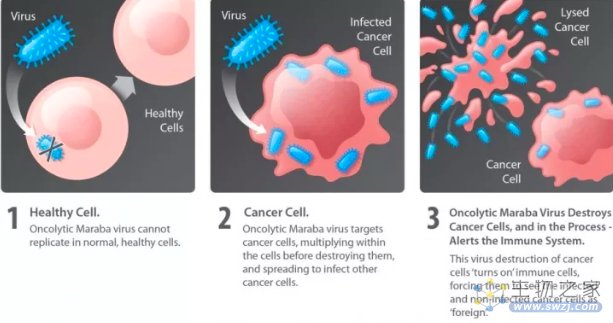
溶瘤病毒(Oncolytic virus,OVs)是指天然存在的、或者基因编辑后,可以有选择性杀灭肿瘤细胞的病毒总称。原则上,肿瘤细胞内的生理代谢环境与正常细胞不同,溶瘤病毒因其特性,可以感染肿瘤细胞,并选择性地在肿瘤细胞内复制,导致肿瘤细胞的溶解和死亡;同时,在正常细胞内不能或者只能少量复制,避免影响正常细胞。
溶瘤病毒疗法就是利用溶瘤病毒这个特点,将其作为抗肿瘤的疗法。溶瘤病毒疗法抗肿瘤特异性强、效果好、副作用小、发展前景广阔,并且有被监管机构批准的先例,例如:
上海三维公司的安柯瑞,被中国药监局于2005年批准,与化疗药物联用治疗鼻咽癌;
安进公司的T-Vec,被美国FDA于2015年批准治疗无法手术切除的复发性恶性黑色素瘤,也是唯一被FDA批准的溶瘤病毒药物;
2021年6月,日本第一三共公司宣布,其研发的Delytact获得厚生劳动省的有条件性限时批准,是全球首款获批治疗脑胶质瘤的溶瘤病毒疗法。
20世纪初,临床医生就观察到癌症病人因为偶然的病毒感染而使肿瘤缩小的现象,推测某些种类的病毒会优先感染杀死肿瘤细胞。于是,在1950年后近20年的时间,利用各种野生型病毒治疗肿瘤的临床试验大量涌现。这是最早的对于溶瘤病毒疗法的尝试。然而,因为野生型病毒疗效欠佳,一直未能发展成为有效的治疗手段。
20世纪90年代后,由于分子病毒学高速发展,使得基因改造溶瘤病毒成为可能,为溶瘤病毒疗法的发展带来了全新的机会,溶瘤病毒疗法的开发进入了第二阶段,例如:Virttu Biologics公司的HSV1716就是以单纯孢疹病毒(Herpessimplexvirus,HSV-1)为基准,去除了神经毒基因ICP34.5而失去了感染神经细胞的能力,进而成为新型溶瘤病毒。
21世纪之后,溶瘤病毒的开发又加入了新元素:将各种外源性的基因加入溶瘤病毒,用以增强溶瘤病毒的选择性和疗效,这开启了这种疗法发展的第三阶段。
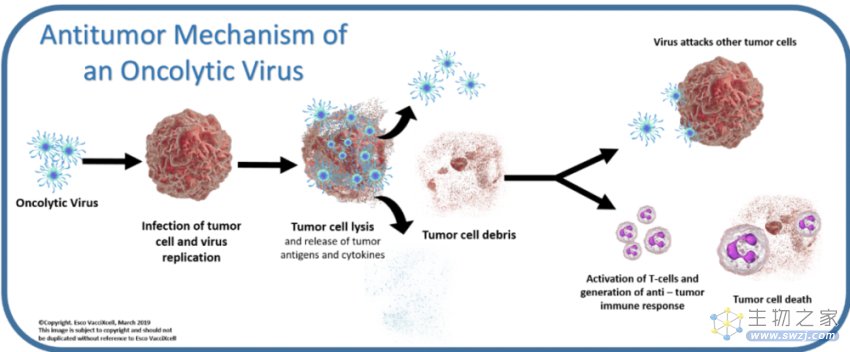
溶瘤病毒杀死肿瘤细胞机理
溶瘤病毒大体可以分为两类:天然病毒株及人为改造的病毒株。天然病毒株指野生型病毒或者自然变异的病毒株,病毒本身毒力难控制,对肿瘤细胞的杀伤能力有限,更重要的是,容易激活人体免疫系统而被人体直接清除,无法达到杀灭肿瘤的效果。而人为改造的溶瘤病毒则可克服天然病毒株的一些缺点,如可剔除某些致病基因、插入外源性治疗基因、甚至可加入新的抗癌机制,因此更受欢迎。
若以遗传物质种类进行分类,溶瘤病毒可分为DNA病毒与RNA病毒:DNA溶瘤病毒包括腺病毒、痘病毒、疱疹病毒等;而RNA溶瘤病毒则有呼肠孤病毒、麻疹病毒、新城疫病毒等。现在比较常用的溶瘤病毒为腺病毒、单纯疱疹病毒、呼肠孤病毒、柯萨奇病毒、痘病毒、逆转录病毒、新城疫病毒等。以腺病毒、单纯疱疹病毒、痘病毒以及柯萨奇病毒等作为载体的溶瘤病毒疗法已处于临床试验阶段。
溶瘤病毒作用机理分为三个部分:
1. 溶瘤病毒可引发病毒介导的肿瘤杀伤。如同病毒感染细胞的一般过程,溶瘤病毒可以选择性地在肿瘤细胞内复制,利用肿瘤细胞内的原料、能量以及空间进行大量复制,最终裂解肿瘤细胞。肿瘤细胞裂解后,释放的大量子代溶瘤病毒,则可以继续感染附近的肿瘤细胞。这个循环过程即可减灭肿瘤细胞;
2. 溶瘤病毒感染肿瘤细胞可以激活人体自身免疫系统,引发全身性抗肿瘤免疫反应。溶瘤病毒侵入肿瘤微环境中之后,会对原有的免疫平衡产生强烈扰动,刺激肿瘤微环境中原有的免疫细胞,启动或加强此微环境中的抗肿瘤免疫反应。同时,溶瘤病毒感染了肿瘤细胞之后,肿瘤细胞可能会释放炎症因子,激发人体固有的免疫反应。而肿瘤细胞被感染后裂解,肿瘤细胞内所有物质释放,此过程也称为全息“抗原释放”。
这些物质就是直接与此肿瘤相关的抗原,促进人体免疫系统对肿瘤抗原识别,激活人体适应性免疫反应。这些激活人体本身免疫系统活跃性的因素,可大大提高免疫系统识别肿瘤的能力,进而调动自身免疫系统来杀死肿瘤细胞;
3. 肿瘤细胞被溶瘤病毒感染后裂解,可以释放细胞毒性穿孔素和颗粒酶,进而杀死附近的肿瘤细胞,扩大杀伤力,这个过程被称为“旁观者效应”(Bystander effect)。
从免疫系统反应机制分析,溶瘤病毒疗法有几个突出的优点:
1. 溶瘤病毒与多种抗肿瘤药物及疗法(包括化疗药物、靶向疗法、细胞疗法)有天然协同性,溶瘤病毒可将无法对其他免疫疗法回应的“冷肿瘤”变成可以对药物回应的“热肿瘤”,且两者联用没有明显叠加的毒性,因此可创造出更优异的抗癌疗法。适应症主要有黑色素瘤、神经胶质瘤、乳腺癌、非小细胞肺癌、结肠癌、膀胱癌、头颈部癌和前列腺癌等;
2. 溶瘤病毒可以通过改造调控,控制其对正常细胞的影响,所以此疗法预期副作用小。现有的临床数据表明:溶瘤病毒与其他疗法相比,总体显示出更好的安全性;
3. 溶瘤病毒的改造也有多种可能,可进一步增强对肿瘤细胞的杀伤力,例如:可将病毒改造成可以传递抑癌基因,或者加入免疫调控功能等;
4. 溶瘤病毒疗法适用于绝大部分实体瘤。中国实体瘤的未满足医疗需求状况与欧美相比更为严峻,鉴于此,溶瘤病毒疗法在中国市场潜力更大。
溶瘤病毒疗法临床试验进度显示,现阶段绝大多数候选产品处在临床前与早期临床阶段,处于临床后期阶段以及已上市的产品屈指可数。上市产品尚未出现“重磅炸弹”,安进的T-Vec每年销售大约7000万美元。
溶瘤病毒疗法前景广阔,但技术尚未成熟,在应用上依然面临挑战:
1. 从现有数据分析,溶瘤病毒的疗效还比较弱。溶瘤病毒感染肿瘤细胞且在其中复制的效率有限,肿瘤细胞被溶瘤病毒诱导的细胞坏死或程序性死亡,敏感性也有待提高;
2. 溶瘤病毒对人体本身也是异物,免疫系统可能很快对其产生抗病毒反应,而将溶瘤病毒从体内清除;
3. 溶瘤病毒对肿瘤细胞的选择性有限,同时由于其独特的药物动力学与药物代谢学特性,体内病毒复制往往无法控制,可能引发副作用,对溶瘤病毒给药方式的选择带来影响。
溶瘤病毒疗法多数为肿瘤局部递送,直接将高浓度溶瘤病毒递送到肿瘤周围,让其发挥最大作用,但是也因此降低便利性,并非适合所有病况,所以一定程度上限制了溶瘤病毒疗法的发展和使用。便利性较佳的系统性给药则面临许多核心挑战,例如:溶瘤病毒直接进入循环系统后,浓度会被大大稀释,真正能够渗入肿瘤有限,影响治疗效果。另外,这种疗法也可能导致病毒在人体内稳定性变差、激发人体免疫系统反应被清除,或被血液中抗体中和等。
许多企业在寻求解决溶瘤病毒系统性给药的方案,例如:英国PsiOxus Therapeutics公司,以改造腺病毒作为载体的Enadenotucirev已在美国和欧洲开展了多个静脉系统给药的I期临床试验;公司也与美国百时美施贵宝合作,与纳武利尤单抗联用开展治疗多种实体瘤的临床试验。
溶瘤病毒的另一难点在于生产工艺。不同溶瘤病毒种类有各自特点,因此生产过程必须针对各个病毒的状况进行开发,对于培养条件优化、病毒产量的提高以及纯化方案等问题要逐个解决,难点也各不相同:
例如,啮齿源细小病毒(H1-PV)可以适用于悬浮培养工艺,可在无血清条件下进行生产,有助于提高产量和不受血清源污染的安全性,然而在分离提纯过程成本较高,耗时较长;对于呼肠孤病毒的生产,寻找无动物源细胞培养基则是难点;对于痘病毒,贴壁式培养细胞则是比较常用的生产方法,这对提高产量来说有巨大挑战。因此,针对每一种溶瘤病毒,企业都需要仔细钻研,寻找最合适的生产方法。
溶瘤病毒疗法因为其独特性引起广泛关注。美国安进公司与默沙东在此方面均有布局。
在中国,有多家公司参与研发,包括康万达、滨会生物、亦诺微等,提供相关服务的CDMO企业包括和元生物、源兴基因等。
笔者认为溶瘤病毒疗法处于发展的初级阶段,机遇与挑战并存。期待此疗法在实体瘤治疗中占有重要地位。
笔者基金研究过以下企业,在此举例:
CGOncology在美国加利福尼亚州于2010年成立,专注于溶瘤病毒疗法的研发与转化。
CG0070为核心产品,以腺病毒为载体,针对适应症为非肌肉浸润性膀胱癌(Non-muscle-invasive bladder cancer),单独使用疗法已发展至临床试验III期,临床效果显著。同时,公司与默沙东和百事施贵宝均有合作,将CG0070分别与可瑞达和欧狄沃联用,针对非肌肉浸润性膀胱癌。
2020年3月,与日本Kissei制药就其CG0070达成协定:Kissei制药将获得CG007在中国以外亚洲地区(含日本)的独家开发和商业化权利,交易价值最高达1.4亿美元;此外,加上专利使用费,包括1000万美元的许可费和3000万美元的股权投资。































