在新冠疫情期间,mRNA疫苗临危受命并为世界交出了一份令人满意的答卷。而今年的诺贝尔生理学或医学奖也授予了两位在mRNA疫苗上做出突破性贡献的先驱,表明该技术在医学领域的重要性得到了广泛认可。
当然,mRNA疗法的潜力远不止于传染病疫苗,它是一种非常灵活和多功能的平台,可以用于多种不同的治疗应用,例如癌症疫苗、遗传疾病治疗、蛋白质替代疗法等等。近几年来,专注于mRNA疗法开发的生物医药公司也在不断探索mRNA疗法的疆界,利用mRNA在体内生成嵌合抗原受体(CAR)细胞疗法是其中一种新的尝试。在今天的这篇文章中,药明康德内容团队将结合公开资料为大家介绍该领域的部分新进展。
大胆的创新:直接在患者体内制造CAR细胞
自CAR细胞疗法诞生以来,就创造了许多医疗奇迹,其中最著名的就要数全球首位接受CAR-T细胞疗法的孩子的故事——曾患致命白血病的Emily至今已无癌生存超过11年。自那时起,“一次治疗,永久治愈”成为了细胞疗法的最高追求,不断鼓舞着创新者们投身其中。然而,这类疗法的局限性也非常多,例如制造过程复杂、对细胞供体的健康状况也有一定要求、高度个体化难以开发通用型现货疗法,以及对实体肿瘤的效果远不如血液癌症等。
科学家和新药研发人员们一直在尝试利用各种策略突破这些瓶颈,截至目前收效仍然有限。但这一次,结局可能不一样——利用mRNA技术直接在患者体内制造CAR细胞的大胆创新将有望一次性解决以上所有痛点,大幅提高此类疗法的可及性。更令人感到高兴的是,利用这种策略的创新疗法已在临床前实验中取得积极结果,有疗法已计划在2024年进入临床阶段。
在不久前召开的癌症免疫治疗学会年会(SITC)上,专注于通过mRNA递送技术来变革细胞疗法的Capstan Therapeutics公司表示,他们已成功利用脂质纳米颗粒(LNP)递送mRNA在人源化的小鼠体内制造出了CAR-T细胞。这些在体内生成的CAR-T细胞作用强大,根除了小鼠体内的原代B细胞和白血病细胞。该结果为在患者体内重编程免疫细胞为CAR细胞提供了支持。
那这种疗法具体是如何操作的呢?简单来说,这种新兴的疗法基本上是通过直接向患者体内注射含有特定mRNA的生物制品来发挥作用的。首先,科学家们会设计并合成特定的mRNA分子,这些mRNA包含编码用于识别和攻击癌细胞的CAR的遗传信息。为了让本身较不稳定且不能轻易穿过细胞膜的mRNA分子能够顺利到达靶细胞,研发人员们会利用LNP有效地包裹mRNA,然后使用静脉输注的方式让这些LNP进入人体。当免疫细胞吸收LNP后,mRNA将被释放并指导免疫细胞生产CAR蛋白,这样就能达到在患者体内生产CAR细胞的目的了。
这种方法的好处非常明显,它省去了从患者体内分离细胞、在体外进行工程化改造的繁琐过程。此外,传统细胞疗法的使用过程中还需要化疗,并有可能带来一系列的副作用。而体内生成的细胞疗法则无需这一步骤。在临床使用方面,这种创新的体内细胞疗法有望成为一种现货型通用疗法,不仅使用方便,也依然能够对患者自己的细胞进行改造,并为患者提供与现有的个体化细胞疗法同等的获益。
突破血液肿瘤应用限制
以往的细胞疗法通常在血液癌症中的疗效较好,这是因为治疗性的免疫细胞能够与血液中的癌细胞充分接触,便于其杀伤癌细胞。而一些实体肿瘤的肿瘤微环境不利于T细胞进入,如何突破实体肿瘤的防线成为了细胞疗法的一大难题。
一些科学家发现,免疫细胞中的巨噬细胞和其他骨髓细胞并不会被肿瘤微环境拒之门外,因此,利用这类细胞开发细胞疗法将是一个突破口。一旦这些接受改造过的CAR免疫细胞浸润了肿瘤,它们不仅能够自己杀伤肿瘤细胞,还将招募其它强大的免疫细胞(例如T细胞和NK细胞)一起对肿瘤细胞进行围剿。
Carisma Therapeutics与Moderna合作开发的创新疗法CT-0508针对的就是巨噬细胞,该疗法将Carisma公司的CAR-巨噬细胞(M)平台与Moderna的mRNA和LNP技术相结合,能在体内生成CAR-M。在Carisma报告的数据中,他们已成功利用mRNA/LNP技术在小鼠体内生成了CAR-M细胞,使小鼠体内皮下和全身转移的实体肿瘤消退。安全性方面,实验动物对CT-0508重复给药的耐受性良好,没有表现出毒性迹象。不过,Carisma和Moderna均未透露这项候选疗法何时会开展首次人体研究。
除了用于治疗癌症,CAR细胞疗法还可治疗其它由于细胞异常导致的疾病。Capstan Therapeutics专有的靶向脂质纳米颗粒(tLNP)技术通过将LNP与重组蛋白结合剂(如单克隆抗体)偶联,能够介导细胞种类特异性的吸收,而通过设计疾病特异性的mRNA,它们可以对导致疾病的异常细胞发起攻击。
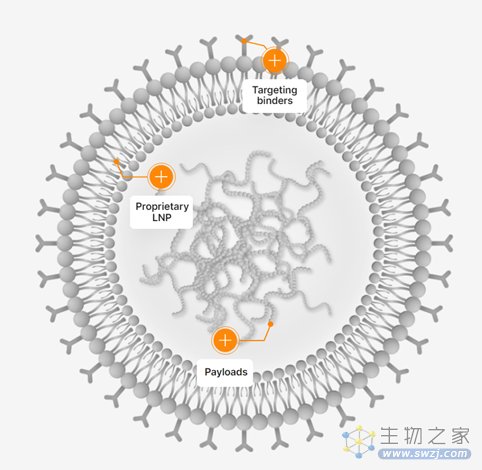
▲tLNP示意图(图片来源:Carisma Therapeutics官网)
此前,该公司已利用其tLNP递送mRNA,成功在心力衰竭的小鼠体内产生了抗纤维化CAR-T细胞。这些CAR-T细胞能够消除心脏纤维化细胞,导致纤维化的显著减少和心脏功能的改善。这项研究表明,CAR-T细胞的体内生成有望成为治疗各种疾病的治疗平台。
不过,由于mRNA只存在于细胞质中,不会整合到患者的基因组里,并且会在细胞分裂时自然降解,因此这些CAR-T细胞在体内存在的时间是短暂的。如果需要此类疗法能持续发挥作用,可能需要多次重复给药。
改善mRNA稳定性
现有技术下,mRNA分子的稳定性仍然不高,因此每个分子能够生成的治疗性蛋白数量有限,很多疗法需要将高剂量的mRNA药物反复注射到患者体内几个月甚至几年来维持蛋白的表达水平。
科学家们发现,一种在哺乳动物细胞中天然存在的RNA——环形RNA为这些挑战提供了独特的解决方案。与线形RNA相比,环形RNA的一大优势是稳定性,它的结构让它们能够避免被先天免疫系统和核酸外切酶识别,不但显著降低了免疫原性,而且具有更高的稳定性。不仅如此,与线形RNA相比,环形RNA折叠产生的构象更为小巧,使用同样的LNP可以装载更多的环形RNA,提高RNA疗法的递送效率。
Orna Therapeutics是一家致力于开发环状RNA疗法的生物医药公司,其内部管线的主攻方向是利用环形RNA的稳定性,通过在T细胞中引入表达CAR的环形RNA,在人体内直接生成CAR-T细胞疗法。看中了环形RNA的广阔潜力,默沙东(MSD)于2022年与Orna公司达成了超35亿美元的研发合作,将共同发现和开发基于环形RNA的多个研发项目,包括在传染病和肿瘤学领域的疫苗和疗法。
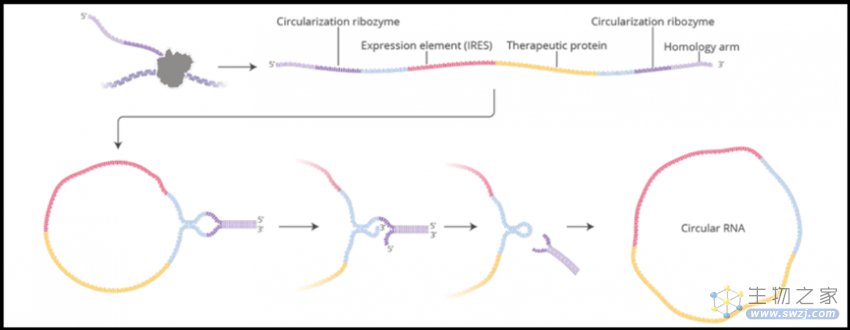
▲Orna公司环状RNA的生成过程(图片来源:Orna公司官网)
在2023药明康德全球论坛上,该公司首席执行官Tom Barnes博士表示,RNA是一个非常令人兴奋的领域。“但疗法的递送仍然是需要解决的重大挑战。”比如在体内生成CAR-T细胞,就要考虑如何将编码CAR的mRNA递送精准地递送到免疫细胞中。
去年,Orna公司首次公布了这一疗法在动物模型中的概念验证数据,在小鼠模型中,其oRNA-LNP复合体能够达到清除癌细胞的效果。而在啮齿类动物和非人灵长类动物中进行的其它研究让Orna有信心将这一成功转化到人体试验中。

▲Orna公司首席执行官Tom Barnes博士在2023药明康德全球论坛上分享洞见
Orna的首席科学官Robert Mabry博士表示,他们的疗法仍然需要每2-3周给药一次。不过这种作用短暂的疗法的好处是,相比于传统的大剂量单剂量CAR-T细胞疗法,更容易预防可能会危及生命的严重细胞因子释放综合征。该公司已计划于2024年开展其可在人体内直接生成CAR-T细胞的环状RNA疗法ORN-101的首个人体试验。
随着mRNA疗法的不断发展,我们正在见证一个医学创新的新时代——通过直接在患者体内制造CAR细胞,有望克服传统细胞疗法的多个限制,为更广泛的患者群体提供治疗希望。尽管这些技术仍处于初期阶段,随着更多临床试验的展开,我们期待着这些创新疗法能够在不久的将来为患者带来实际的治疗效果,特别是那些传统疗法无法有效治疗的病例。
参考资料
[1] mRNA’s next trick? Reprogramming off-the-shelf cell therapies for cancer and autoimmune diseases. Retrieved November 14, 2023, from https://endpts.com/mrnas-next-trick-reprogramming-off-the-shelf-cell-therapies-for-cancer-and-autoimmune-diseases/
[2] Orna Therapeutics Unveils Progress of Circular RNA Platform and Improvements in Lead Program ORN-101 at PEGS and ASGCT. Retrieved November 14, 2023, from https://www.prnewswire.com/news-releases/orna-therapeutics-unveils-progress-of-circular-rna-platform-and-improvements-in-lead-program-orn-101-at-pegs-and-asgct-301827960.html
[3] Simnova and Orna Therapeutics Collaborate to Advance Orna's Next Generation Circular RNA Technology in China. Retrieved November 14, 2023, from https://www.prnewswire.com/news-releases/simnova-and-orna-therapeutics-collaborate-to-advance-ornas-next-generation-circular-rna-technology-in-china-301714094.html
[4] Carisma Presents Pre-Clinical Proof of Concept for in vivo CAR-M using mRNA platform in collaboration with Moderna at SITC. Retrieved November 14, 2023, from https://www.prnewswire.com/news-releases/carisma-presents-pre-clinical-proof-of-concept-for-in-vivo-car-m-using-mrna-platform-in-collaboration-with-moderna-at-sitc-301972835.html
[5] Varghese B, Mori S, Pierini S, et al1514 In vivo CAR-M: redirecting endogenous myeloid cells with mRNA for cancer immunotherapyJournal for ImmunoTherapy of Cancer 2023;11:doi: 10.1136/jitc-2023-SITC2023.1514
[6] Reiss K, Mortimer J, Pohlmann PR, et al635 A phase 1, first in human (FIH) study of autologous macrophages engineered to express an anti-HER2 chimeric antigen receptor (CAR) in participants (pts) with HER2 overexpressing solid tumorsJournal for ImmunoTherapy of Cancer 2023;11:doi: 10.1136/jitc-2023-SITC2023.0635
[7] BioNTech Presents Positive Phase 1/2 Data Update for CAR-T Cell Therapy Candidate BNT211 in Advanced Solid Tumors at ESMO Congress 2023. Retrieved November 14, 2023, from https://www.globenewswire.com/news-release/2023/10/23/2764948/0/en/BioNTech-Presents-Positive-Phase-1-2-Data-Update-for-CAR-T-Cell-Therapy-Candidate-BNT211-in-Advanced-Solid-Tumors-at-ESMO-Congress-2023.html
[8] Capstan Therapeutics to Present Preclinical Data at SITC Demonstrating Rapid Anti-Primary B Cell and Anti-Tumor Activity in Mice with Proprietary Targeted Lipid Nanoparticles Delivering an Anti-CD19 CAR mRNA Construct. Retrieved November 14, 2023, from https://www.businesswire.com/news/home/20231031264744/en
[9] mRNA shot spawns CAR-T cells in the body to repair heart disease damage. Retrieved November 14, 2023, from https://www.fiercebiotech.com/research/mrna-shot-car-t-therapy-body-repair-heart-disease-damage-university-pennsylvania































