“不节食不运动,轻轻松松瘦20斤,每周仅注射一次”,这样的宣传语怎能让人不心动?
于是乎,司美格鲁肽成为了众多减肥人士梦寐以求的神药,甚至多国陷入了供应短缺的状态。
司美格鲁肽的减肥效果究竟有多“神”?
“网红减肥神药”的一炮而红,还要回溯到特斯拉CEO 埃隆·马斯克在社交媒体上晒出的自己“暴瘦”的图片——在度假照被嘲笑肥胖后,马斯克仅用了一个月的时间就成功减去20磅(约9kg)!
而他自曝成功减肥的秘诀是:禁食与Wegovy(活性成分:司美格鲁肽 Semaglutide)。

马斯克减肥前后对比图
事实上,司美格鲁肽最初被批准用于降血糖。作为新型长效胰高糖素样肽-1(GLP-1)类似物,司美格鲁肽能有效地抑制胰高血糖素的释放,从而间接发挥降低血糖的作用。
该药物的一大优点在于:体内半衰期在1周左右,因此能实现一周给药一次。凭此,“一周打一次”的司美格鲁肽迅速取代了上一代降糖药,并于2021年4月在我国上市。

司美格鲁肽能“跨界”减肥的原理并不复杂,或者说其控制体重的作用算是“顺带”——因其能够模拟胰高血糖素的作用,增加了人体对胰岛素的敏感性;在此基础上,饭后的饱腹感提升了,胃排空的速率减慢了,自然能够减少饥饿感、热量摄入以及体重。
不可否认的是,司美格鲁肽用于减肥的效果,短时间来说确实是显著的。
早在2021年,NEJM发布的全球性重磅临床试验显示:仅需每周给药一次2.4mg,在68周的持续用药之后,司美格鲁肽使得肥胖者的体重降低了15.3kg!
此外,JAMA上的研究还将司美格鲁肽的减肥效果与另一常见减肥药“利拉鲁肽”进行了对比,结果发现,使用司美格鲁肽的参与者的体重平均降低了15.8%,显著优于利拉鲁肽组的6.4%。
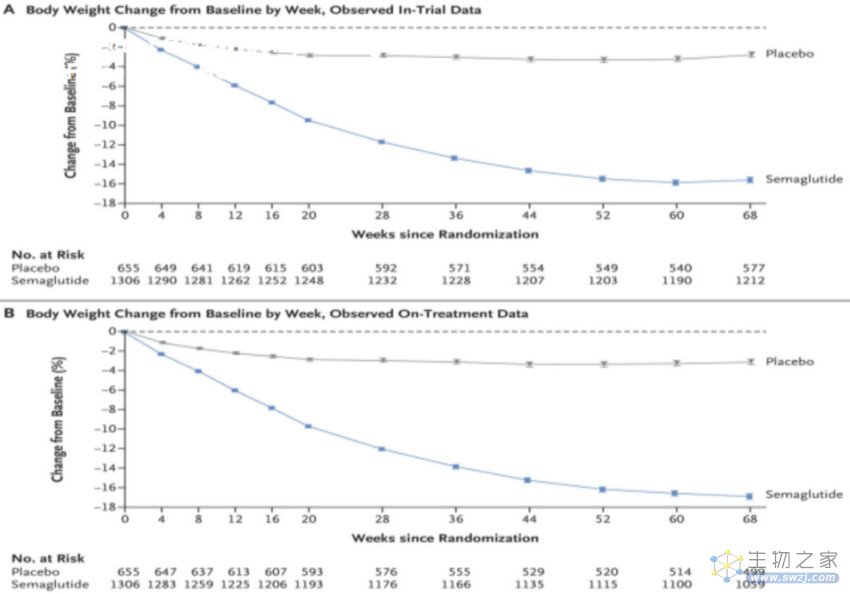
试验组与对照组的体重变化情况(图源:NEJM)
人们使用抗肥胖药物的持久性如何?
但除了药效之外,一个更令人在意的问题是:类似于司美格鲁肽的抗肥胖药物(AOM)持久性如何?为什么人们无法坚持服用减肥药呢?
为了回答这一问题,来自美国克利夫兰医学中心的研究人员调查了多种AOMs的用药持久性以及无法坚持用药的原因。结果显示:随着随访时间的延长,坚持服用AOMs的比例显著下降,从3个月的44%降低到1年时的19%。
为什么还有一大半的人放弃服用该药物呢?这是本研究试图回答的问题。

https://doi.org/10.1002/oby.23952
研究者从俄亥俄州和佛罗里达州的大型卫生系统中2015年至2023年的电子健康记录里筛选出符合纳入标准的研究对象——最终确认了1911名患者,体重指数(BMI)≥30kg/m^2,且在该时间段内首次使用AOM。
其中,AOMs为FDA批准的、用作慢性体重管理的药物以及剂型,包括芬特明-托吡酯、纳曲酮-安非他酮、奥利司他、司美格鲁肽注射液2.4mg和利拉鲁肽注射液3mg。
整个队列的统计显示,有34%服用纳曲酮-安非他酮,26%服用芬特明-托吡酯,25%注射了司美格鲁肽,14%注利拉鲁肽以及0.9%的奥利司他。
研究者在随访期间观察到,3个月时,整个队列中仍有44%的受试者在坚持使用AOM药物;到了6个月,该比例降低至33%;而在1年之后,仅剩19%的患者还在坚持服用AOM。
具体来说,不同药物的持续率差异很大。比如,在3个月和6个月时,司美格鲁肽有着最高的持续率,分别为63%和56%,其次是利拉鲁肽的52%和37%。但在服用药物一年后,纳曲酮-安非他酮的持续率仅为10%,即使持续率最高的司美格鲁肽,也下滑一半以上,降至40%。
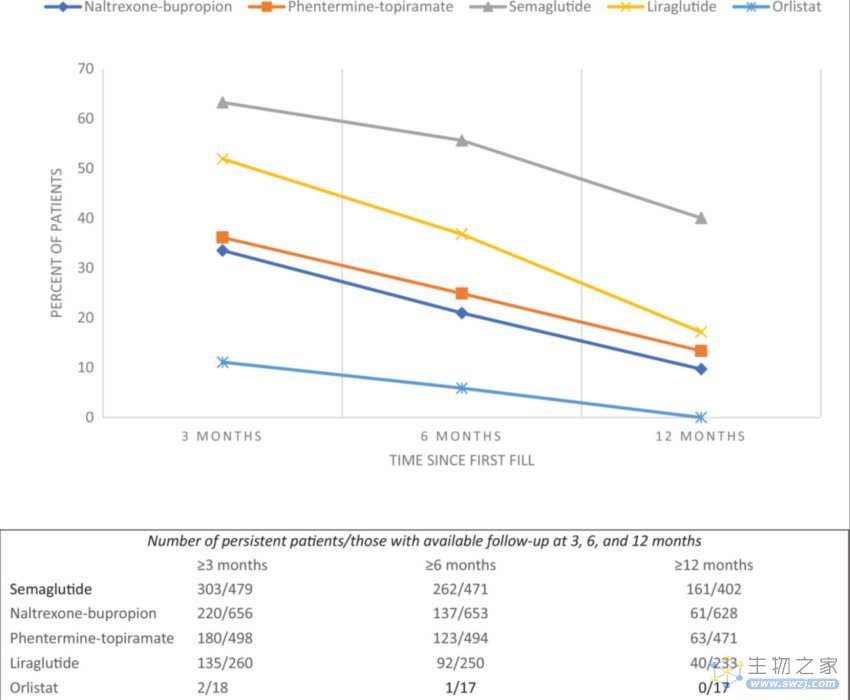
不同药物的坚持用药占比
为什么人们会停止使用AOM呢?
首先,AOM并不平价,甚至算得上高昂,从每月200美元(芬特明-托吡酯)到1300美元(3.0mg利拉鲁肽和2.4mg司美格鲁肽)不等。而这些AOMs大多不属于医保报销的范畴,尤其是昂贵的新一代减肥药——胰高糖素样肽-1受体激动剂(GLP-1RA),相当于要“自费”减肥。此外,随着减肥神药的“一炮而红”,某些国家的司美格鲁肽甚至出现了短缺的现象,一定程度上也限制了患者获取药物的能力,导致AOMs的停用。
其次,除了现实因素之外,司美格鲁肽等GLP-1药物可能引起的不良反应,也受到了越来越广泛的关注。此前,JAMA上刊登的、由哥伦比亚大学医学院科研人员开展的研究,给了大众“当头一棒”——包括司美格鲁肽在内的GLP-1激动剂恐存在一定的不良反应,与胰腺炎、胃轻瘫以及肠梗阻等胃肠道疾病的风险增加有关。
该研究发现,与使用安非他酮+纳曲酮药物进行减肥的相比,两种GLP-1激动剂司美格鲁肽和利拉鲁肽诱发的4种胃肠道不良反应的发病率均更高,包括胆道疾病(比如胆囊炎、胆结石和胆总管结石)、胰腺炎(包括胆结石性胰腺炎)、肠梗阻和胃痉挛。
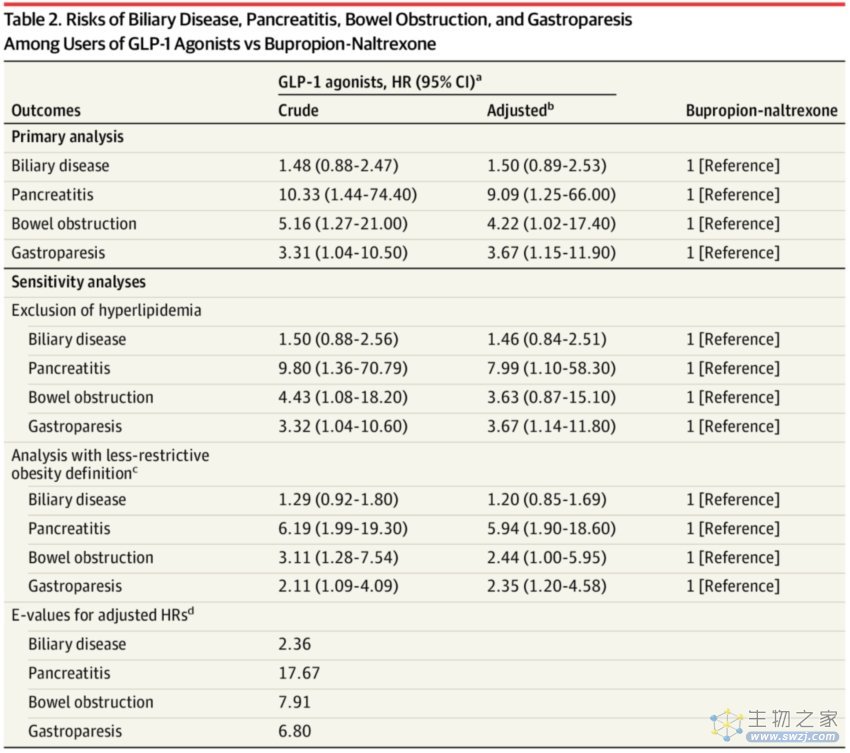
GLP-1激动剂与安非他酮-纳曲酮使用者的胃肠道疾病发生风险
FDA通报的最常见胃肠道不良反应包括:恶心、呕吐、腹泻、腹痛、消化不良、食欲下降等等,更有甚者可能会出现肠梗阻、胃轻瘫等更为严重的疾病。JAMA上刊登的另一项研究也对司美格鲁肽的副作用进行了报道,结果显示,使用司美格鲁肽治疗组出现胃肠道副作用的概率高达84.1%。
第三,也是很关键的一点是,司美格鲁肽并非一打就瘦的“傻瓜针”,而需要配合饮食以及生活方式的管理。在停药之后,很容易出现反弹的现象——一项临床试验显示,在接受司美格鲁肽治疗的参与者停药一年后,减轻的体重恢复了超过50%。
也就是说,坚持使用司美格鲁肽,确实可以保证体重的减轻;但一旦干预停止,反弹的可能性恐怕会更高。
事实上,人体产生的内源性GLP-1与这些注射的人造GLP-1具有一定的差异。前者会在餐后释放,但不会持续很长时间,且会被身体迅速代谢掉;相比之下,后者的活性往往更高(甚至是内源性GLP-1的10倍),持续时间也会更长,让患者在注射后维持更长久的饱腹感。“吃得少、不易饿”,自然也会更瘦。
然而,由于人为的干预,即外源性GLP-1的增加,身体检测到更高水平的“假”GLP-1后,合成的内源性GLP-1会随之减少。在突然停药之后,体内原本高水平的GLP-1骤然下降,饥饿和食欲会“报复性回归”,导致体重的迅速反弹。
看来“坐躺瘦”的美梦在现阶段还是很难实现的,在用药之后的体重维持才是更大的考验!
参考资料:
[1] Gasoyan H, Pfoh ER, Schulte R, Le P, Rothberg MB. Early- and later-stage persistence with antiobesity medications: A retrospective cohort study. Obesity (Silver Spring). 2023 Dec 6. doi: 10.1002/oby.23952. Epub ahead of print. PMID: 38053443.
[2] Khoo TK, Lin J. Once-Weekly Semaglutide in Adults with Overweight or Obesity. N Engl J Med. 2021 Jul 1;385(1):e4.
[3] Rubino DM,et al. Effect of Weekly Subcutaneous Semaglutide vs Daily Liraglutide on Body Weight in Adults With Overweight or Obesity Without Diabetes: The STEP 8 Randomized Clinical Trial. JAMA. 2022 Jan 11;327(2):138-150.
[4] Sodhi M, Rezaeianzadeh R, Kezouh A, Etminan M. Risk of Gastrointestinal Adverse Events Associated With Glucagon-Like Peptide-1 Receptor Agonists for Weight Loss. JAMA. Published online October 05, 2023. doi:10.1001/jama.2023.19574































