骨骼不仅仅是人体支架和矿盐储备器,它还是人体重要的内分泌器官。骨骼(骨髓)能主动合成和分泌多种生物活性因子,如骨调节蛋白、生长因子和炎症因子等,通过自分泌、旁分泌和内分泌的方式,参与调控骨骼和机体的稳态平衡。
骨质疏松是一种由于骨量丢失与降低、骨组织微结构破坏、骨脆性增加,导致患者容易出现骨折的全身代谢性骨病。50岁以上的男性五分之一患有骨质疏松症,全球2亿妇女受到骨质疏松的威胁。全球每年会有900多万人因为骨质疏松而发生骨折,相当于全球每3秒发生一次骨质疏松症骨折。骨折愈合困难导致的残疾是老年人常见的死亡原因。目前,增进成骨愈合和拮抗骨质丢失的特效药依旧缺乏,寻找新的生物学靶标因子是成为研究热点。
2023年4月由桂林医学院广西肿瘤免疫和微环境的陈琍研究员和南丹麦大学医院合作,发表在《自然通讯》(Nature Communications)上的一项新研究发现:抑制骨和骨髓干细胞分泌因子KIAA1199会增强骨骼干细胞向成骨细胞的分化,并促进骨骼再生和骨骼愈合。

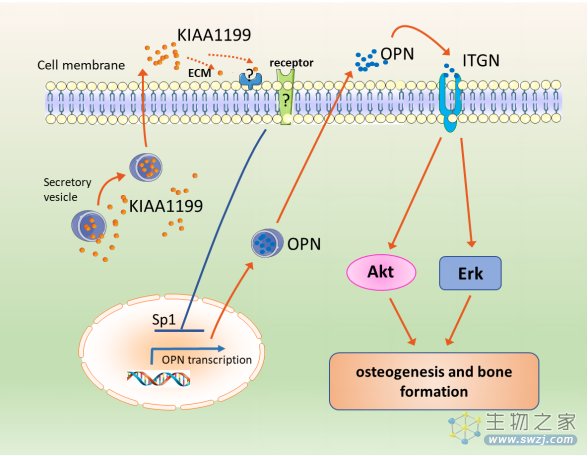
研究人员发现:在临床病人中,血浆中的KIAA1199水平与骨质疏松性骨折风险正相关,而人体骨髓基质干细胞中KIAA1199的表达水平与其干细胞的成骨分化潜能负相关;敲除KIAA1199的人类骨髓干细胞增强了体外成骨细胞分化和体内异位骨形成;KIAA1199基因敲除小鼠的骨量和生物力学强度增加,骨形成率也增加,它们还表现出加速骨损伤愈合,并防止卵巢切除术引起的骨质流失;在细胞机理上,KIAA1199调控骨重塑中的成骨细胞分化和破骨细胞分化;从分子水平上,KIAA1199调控骨桥蛋白(Osteopontin)表达,通过整合素(Integrin)调控AKT和MAPK信号途径来完成了对成骨分化的调节。这个发现对于靶标干细胞因子治疗骨质疏松症和其他低骨量疾病的新药开发具有重要意义。
原文链接:https://www.nature.com/articles/s41467-023-37651-1































