前列腺癌是全球男性第二常见的癌症,也是全球男性肿瘤死亡的第五大病因。
并且,目前晚期前列腺癌患者预后特别差,5年生存率仍然很低。尽管PARP抑制剂联合雄激素受体抑制剂在晚期前列腺癌治疗方面取得了不错进展,但对于患者来说,对新的治疗方案仍存在着巨大的未满足医疗需求。
据《Nature Reviews Drug Discovery》一篇文章分析,2020年前列腺癌市场112亿美元,到2029年这一数字将增至301亿美元。
不过,面对如此巨大的市场,开启癌症治疗新时代的免疫疗法,绞尽脑汁也没能切入这一赛道。哪怕是PD-1抑制剂中的王者K药,面对前列腺癌也是四战四败。
如果时间倒回到十多年前,彼时的研究人员或许不会想到,前列腺癌的战役会打得如此艰难。毕竟,彼时全球首个癌症疫苗,就诞生于前列腺癌领域。
看来,不管是宏大的故事开头,还是耀眼的药王头衔,都与一款药物最终的临床成功没有太大关系。
屡战屡败的免疫疗法
前列腺癌的生长和进展都依赖雄激素,所以目前前列腺癌的治疗,主要是通过雄激素剥夺疗法,阻断体内雄激素(睾酮)的供应。
但是,对一部分患者来说,即便经过雄激素剥夺疗法治疗后,患者体内睾酮水平已经很低,但肿瘤却仍然不断进展,成为转移性去势抵抗性前列腺癌(mCRPC),癌细胞扩散至前列腺以外。
在临床试验环境中,mCRPC患者的总生存期约为3年,而在现实中,这一时间更短。大约一半的mCRPC患者可能只接受一种有效的治疗,后续治疗的益处逐渐减少。
mCRPC是一种更严重、更晚期的癌症,预后更差。因此,前列腺癌患者亟需新的治疗方案。
这便是免疫疗法进军前列腺癌的机会所在。实际上,早在2010年,免疫疗法就打响了征战前列腺癌的第一枪。彼时,全球范围批准的第一款癌症治疗疫苗sipuleucel-T获批上市,用于治疗前列腺癌。
临床试验结果显示,比起对照组,sipuleucel-T将患者的总生存期延长了4.1个月。这一数据算不上惊艳,且仅局限于无症状或症状轻微的早期CRPC人群。
本来以为这会是免疫疗法进军前列腺的开始,没想到开局即巅峰。此后其他的免疫疗法,无论是CTLA-4抑制剂还是PD-1抑制剂,在前列腺癌的征战中,大都以失败告终。
拿CTLA-4抑制剂Ipilimumab来说,在针对mCRPC患者的两项III期研究中,其都未能显示出总生存期的改善。
或许你会说,CTLA-4抑制剂还不够强,不足以代表免疫疗法的整体水平。那么,免疫之王K药的失败,或许更能说明问题。
在名为KEYNOTE-199的临床试验中,即便是针对PD-L1阳性mCRPC患者,K药的单药客观缓解率也仅有5%。
当然,面对前列腺癌这一潜力巨大的市场,K药不会轻易放弃。K药又展开了与PARP抑制剂、多烯紫杉醇、雄激素剥夺疗法、恩扎卢胺与雄激素剥夺疗法的多项联合疗法。
遗憾的是,这些联合疗法的临床试验都没有得到有意义的结果。
2022年3月15日,K药与PARP抑制剂奥拉帕利联合疗法,用于mCRPC患者的III期临床试验不仅没能展示出更好的效果,还出现了不良事件发生率提高的情况。
要知道,K药和PARP抑制剂都属于各自领域的佼佼者,其中PARP抑制剂已被批准单药治疗前列腺癌,但如今强强联合却未能展示出1+1>2的效果,这也让市场对于免疫疗法在前列腺癌中的作用存疑。
这次的失败还只是一个开始,随后在K药联用多西他赛、恩扎鲁胺和雄激素剥夺疗法治疗前列腺癌的III期临床试验,都以失败告终。
就在2月28日,K药又迎来了的第四次失败。至此K药,对于前列腺癌的征战争战全军覆没。
免疫疗法路上的“拦路虎”
免疫疗法,打开了癌症治疗一扇新的大门,成千上万患者因此受益。但免疫疗法却在前列腺癌领域久攻不下,限制免疫疗法在前列腺癌发挥作用的因素是什么?看上去,前列腺癌自身的复杂性质,是免疫治疗征战前列腺癌道路上最大的“拦路虎”。
首先,前列腺癌具有较低的肿瘤突变负荷。
肿瘤突变负荷,简单理解也就是癌细胞中突变数量的多少。这一指标与免疫疗法的反应性强弱有着紧密的关系。
肿瘤突变负荷越高,癌细胞就会表达更多的新抗原。这些新抗原可以被细胞毒性T细胞识别,细胞毒性T细胞又会被免疫检查点抑制剂激活,产生更强大的免疫反应。
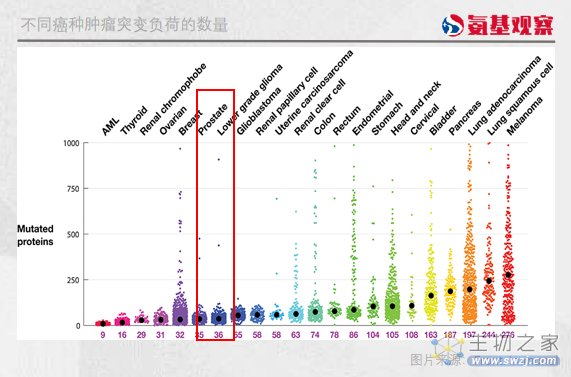
在前列腺癌中,肿瘤突变负荷与非小细胞肺癌、黑色素瘤等其他免疫反应性癌种相比,明显更少。这是前列腺癌对免疫疗法响应率低的原因之一。
其次,前列腺癌为一种冷肿瘤。
我们知道,肿瘤为了能够更好的生存,会为自己打造一片适合生长的土壤,即肿瘤微环境。肿瘤微环境不仅会让周围的细胞产生免疫抑制,同时还会帮助肿瘤细胞逃避免疫攻击。
不过,不同肿瘤的免疫微环境也并不相同。我们可以根据肿瘤微环境的差异,将肿瘤分为热肿瘤、冷肿瘤。其中,热肿瘤中T细胞浸润相对丰富,免疫检查点在这种环境下能产生更强的反应性。而冷肿瘤T细胞缺乏,对于免疫疗法的反应性较弱。
很遗憾,前列腺癌就属于后者。前列腺处于泌尿道的位置,在这个位置上会接触到不少传染性生物,为了不对这些生物过度反应,前列腺组织中本就不会存在太多的免疫细胞。这也就导致,前列腺癌很难对免疫疗法产生较强的反应。
当然,除了上述因素,PD-1/PD-L1表达水平,免疫微环境中的慢性炎症等因素,也都或多或少的影响着免疫治疗对于前列腺癌的效果。
从失败中汲取前进力量
创新药研发,或许是最能体现“失败是成功之母”这一真谛的领域。
拿如今叱咤药坛的“风云药物”mRNA疫苗来说,今日之发展也是在数次失败的经验积累上得到的。
前列腺癌药物的研发也会如此。虽然,眼下免疫疗法还未找到突围的方向,但只要仍有人在为之探索,就一定会有找到方向的时刻。
实际上,打头阵的免疫联合疗法,正在撕开这无尽黑夜。比如,癌症疫苗和其他免疫检查点抑制剂的组合疗法。
PROSTVAC-VF是一种以PSA(前列腺特异性抗原)为靶点的病毒疫苗。虽然在三期临床试验中,它的临床数据不如人意,但在与免疫抑制剂联用后,展示出了潜力。
2022年6月,NCI、NIH公布了这款疫苗联合O药+Y药治疗mHSPC(转移性激素敏感性前列腺癌)的一项1期试验的临床数据。结果显示,在中位随访的22.6个月时间里,中位总生存期(OS)尚未达到,2年OS率为75%。安全性方面,治疗过程中没有发生4级或4级以上的不良反应事件。
再比如,BioNTech的BNT112也是一款治疗前列腺癌的mRNA疫苗,目前其正在1/2期临床试验中单药或与PD-1抑制剂联用,治疗前列腺癌患者。
此外,双抗也在试图打败前列腺癌。比如,安进研发了一款PSMAxCD3双抗AMG-160,其一只手与CD3结合抓住T细胞,另一只手抓住前列腺癌表面的PSMA抗原,使得T细胞与癌细胞聚集在一起,T细胞得以对前列腺癌细胞发动攻击。
在I期临床研究中,68.6%的患者在所有剂量组中显示PSA下降。单药之外,AMG 160与K药联用的研究也正在进行。
对于免疫疗法如何打败前列腺癌的问题,我们还没有标准答案,但从失败中汲取前进的力量,驱动着药企不断探索。当黑夜逐渐褪去,免疫疗法也将找到出路,为前列腺癌症患者带去新的希望。































