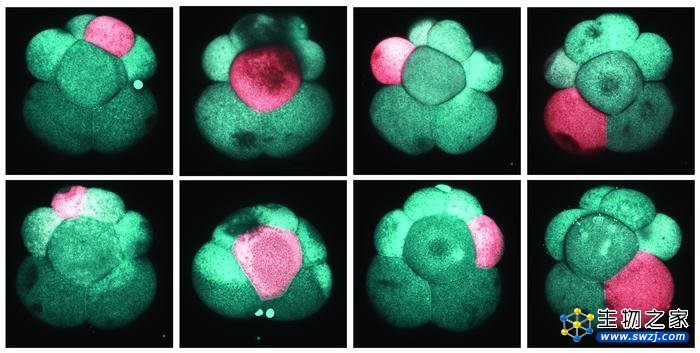
导读:具备再生能力的动物的一个共同特征是成年体内存在多能干细胞。当动物受伤时,这些细胞负责重新制造缺失的身体部位。
干细胞是一个生物学奇迹,它们可以修复、恢复、替换和再生细胞。在大多数动物和人类中,这些细胞仅限于再生它们所分配的细胞类型,如毛囊干细胞只会再生头发,肠道干细胞只会补充肠道。
但是,许多远亲无脊椎动物的干细胞群在成年动物中是多能的,这意味着它们几乎可以再生任何缺失的细胞,这一过程被称为全身再生。尽管这些成体多能干细胞(aPSCs)存在于许多不同类型的动物(如海绵、水螅、涡虫、扁虫和一些海鞘)中,但它们再生的机制仍不清楚。
近日,哈佛大学有机体和进化生物学系在Cell期刊发表的一项研究中,研究人员确定了三斑黑豹蠕虫(Hofstenia miamia)形成成体多能干细胞的细胞机制和分子轨迹。
DOI:https://doi.org/10.1016/j.cell.2022.11.008
01
全身切碎能再生
三斑黑豹蠕虫是一种海洋动物,学术名为Hofstenia miamia,它是有史以来全身再生能力最强的动物之一。砍掉三斑黑豹蠕虫的头,另一颗头就会取而代之;剪掉它的尾巴,它会再长出一条来。把蠕虫切成三块,无论是对角斜切还是横切,不出八个星期,就会有三只完全成形的蠕虫。
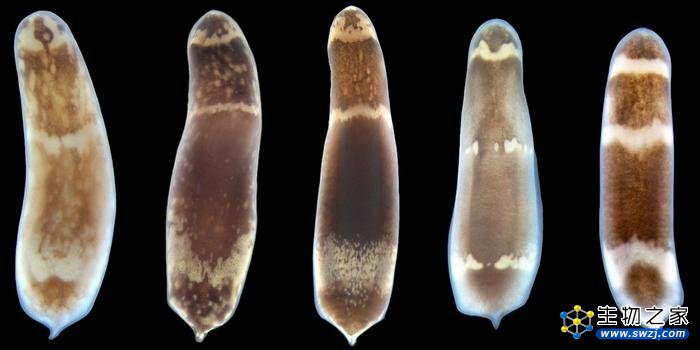
研究人员表示,具备再生能力的动物的一个共同特征是成年体内存在多能干细胞。当动物受伤时,这些细胞负责重新制造缺失的身体部位。通过了解像三斑黑豹蠕虫这样的动物如何制造这些干细胞,可以更好地了解是什么赋予了某些动物再生能力。
研究的资深作者Mansi Srivastava教授多年前在野外收集了三斑黑豹蠕虫。在回到实验室后,他开始制作许多易于研究的胚胎。Srivastava和博士后研究员Lorenzo Ricci在之前的一项研究中开发了一种在H. miami中的转基因方案,这种方法让首席作者Julian O. Kimura能够继续研究这些干细胞是如何形成的问题。
02
追踪胚胎发育过程
研究人员推断蠕虫幼体含有的成体多能干细胞一定是在胚胎发生过程中产生的。Ricci利用转基因技术创造了一种细胞系,通过将Kaede蛋白引入细胞,使胚胎细胞发出荧光绿色。Kaede是光可转换的,也就是说可以用特定波长的激光束照射绿色,将其转换为红色。因此可以用激光照射这些细胞,将胚胎的单个绿色细胞变成红色。

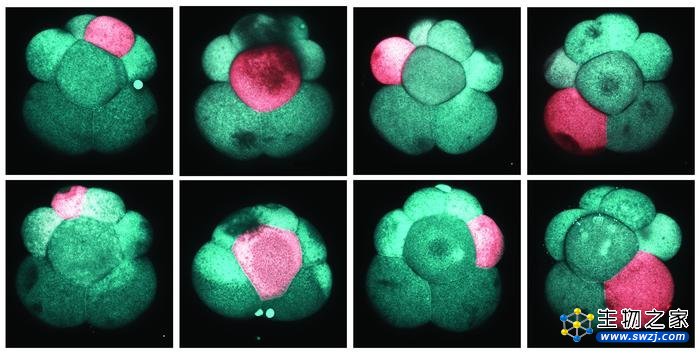
图像显示胚胎的单细胞是如何具体而系统地转化为红色的
随后,Kimura跟踪了胚胎从单细胞分裂到多细胞的发育过程。这些细胞的早期分裂以定型分裂为标志,这说明胚胎细胞以完全相同的模式分裂,这样就可以对细胞进行一致的命名和研究。这也提出了一种可能性,也许每个细胞都有独特的用途。例如,在八细胞期,左上角的细胞可能生成某种组织,而右下角的细胞则生成另一种组织。
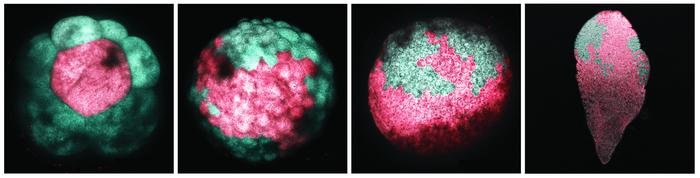
8细胞期胚胎的单个细胞转变为红色
为了确定每个细胞的功能,Kimura对早期胚胎的每个细胞进行了系统的光转换,在八细胞期创建了完整的命运图。在16细胞期的胚胎中,他发现了一对非常特殊的细胞,这对细胞产生了看起来像neoblasts(即成体未分化细胞)的细胞。
为了证明它们产生的是neoblasts,Kimura对这组特殊的细胞进行了试验,命名为3a/3b。他发现,只有这些细胞的后代在再生过程中产生了新的组织。此外,另一个决定性的特性是干细胞中的基因表达水平,干细胞必须表达数百个基因。为了确定3a/3b是否符合这一特性,Kimura选取了3a/3b发光的红色细胞和所有其他发光的绿色细胞的后代,并使用分选机将红色和绿色细胞分开。然后,他应用单细胞测序技术来研究在红色细胞和绿色细胞中分别表达了哪些基因。该数据证实,在分子水平上,只有3a/3b细胞的子代与干细胞匹配。
03
锁定了一组基因
Kimura表示:“这最终证实了我们在我们的系统中找到了干细胞群的细胞来源。但重要的是,了解干细胞的细胞来源能够让我们在细胞成熟时捕获它们,并确定哪些基因参与了制造它们。”Kimura在单细胞水平上生成了一个巨大的胚胎发育数据集,详细说明了从胚胎发育的开始到结束,哪些基因在胚胎的所有细胞中表达。
研究人员最终锁定了一组基因,包括转录因子Hes、FoxO和Tbx,它们可能是多能干细胞形成的非常重要的控制者,并且这些基因的同源物在人类干细胞中发挥着重要作用。研究人员计划继续深入挖掘这些基因在三斑黑豹蠕虫干细胞中的工作机制,以揭示大自然是如何进化出制造和维持多能干细胞的方法的。总之,了解aPSCs的分子调控因子将使研究人员能够在不同物种间比较这些机制,揭示多能干细胞是如何在动物间进化的。
参考资料:
https://www.eurekalert.org/news-releases/973580
https://www.cell.com/cell/fulltext/S0092-8674(22)01420-9#%20
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。































