众所周知,抗生素是指治疗细菌感染的药物,其通过杀死细菌或遏制细菌繁殖来彻底清除它们。研究发现人体在经历抗生素暴露后会发生胃肠道(GI)微生物组变化,例如促炎性群落的富集、包括腹泻在内的GI不适等等。但目前对于GI微生物群如何恢复到治疗前状态的研究还较少。近期,来自麻省大学医学院、纪念斯隆-凯特琳癌症中心等的研究人员在Science Translational Medicine上发表了题为“Commensal antimicrobial resistance mediates microbiome resilience to antibiotic disruption”的研究成果。通过检查临床队列,Bhattarai等人纵向研究了耐多药(MDR)结核病(TB)抗生素治疗对肠道微生物群的长期影响。虽然治疗严重破坏了患者肠道菌群的稳定性,但在6至24个月的治疗完成时,非致病性细菌开始重新繁殖,并逐渐恢复如初。研究证实药物作为一种选择性压力,影响着微生物群的进化动态。

DOI:10.1126/scitranslmed.adi9711
MDR TB治疗会严重破坏粪便微生物组的分类和功能组成
研究招募了24名MDR TB患者(13名男性和11名女性),其中大多数人在之前的标准治疗中失败。图1A为患者粪便和血液样品的收集时间表,包括第0天(治疗前)、2周、1个月、2个月、6个月和治疗完成时的样品。研究人员通过在相同的时间点记录 BACTEC 培养阳性时间(TTP),来测量痰液中的TB细菌载量。图1B中显示,随着治疗,抗生素明显减少了痰中结核分枝杆菌(Mtb)的细菌量(P < 0.001)。
为了研究伴随MDR TB治疗的GI微生物组变化,研究人员通过对患者粪便进行宏基因组测序,确定了其中的微生物组成和基因含量。结果显示,基线或治疗完成时采集的样本与早期样本(2周、2个月和6个月)在物种和功能途径丰度方面存在显著的统计学差异。其中,微生物组多样性从开始治疗后的两周内快速降低,代表着广泛的细菌耗竭,除此之外,致病菌开始扩增,包括Klebsiella pneumoniae, Klebsiella varicola, Escherichia coli等。
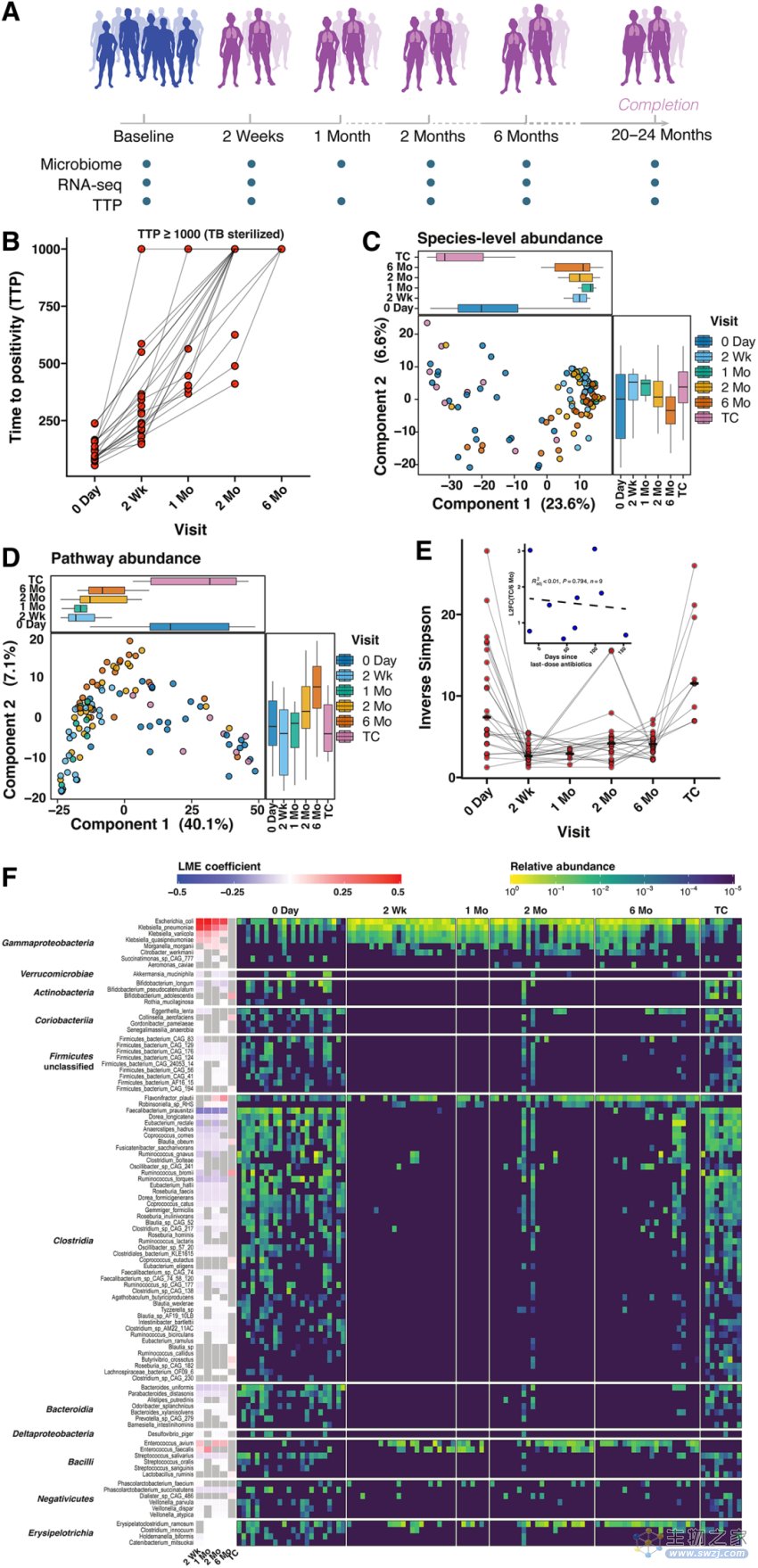
图1. MDR TB治疗清除了患者肺部的结核杆菌,并导致微生物群的暂时性紊乱,而这种紊乱会在停止治疗后恢复
而令人惊讶的是,如图1E中显示,GI微生物组的总体多样性在治疗过程后期反弹至治疗前水平,大多数被抗生素耗尽的物种也在6个月时恢复至治疗前基线,并且在治疗停止时几乎完全恢复代谢活力(图1F),这表明微生物组具有令人惊叹的恢复力。
结核病的炎症消退是病原体杀灭和微生物组扰动的综合效应
研究人员通过建立计算模型,推导出病原体和微生物组依赖性变化的主导效应——抗生素驱动的病原体减少,其伴随着常见炎症(IFN-α、IFN-γ、IL- 6等)、信号转导和转录激活子STAT3、信号传导通路TNF-α等的表达显著降低。其中,高丰度的产短链脂肪酸的梭菌属IV和XIVa(D. longicatena, Erysipelatoclostridium ramosum等)与外周炎症途径减少相关;而高丰度的耐氧菌如Enterobacteriaceae,则与外周炎症、免疫信号传导、TB相关基因的富集相关联。
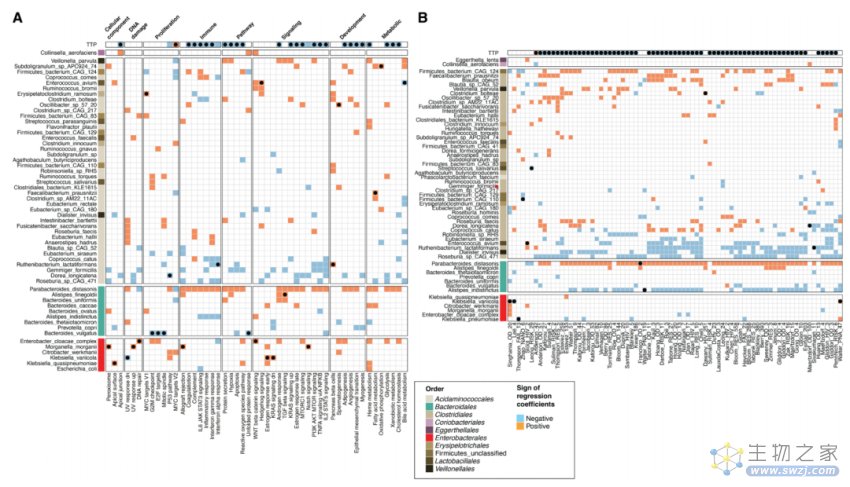
图2. 结核病状态与微生物组扰动、病原体杀灭情况的关联性
总之,研究分析表明,梭菌属IV和XIVa的丰度越高,与菌群失调相关的耐氧菌如Enterobacteriaceae的水平越低,结核病相关外周炎症的缓解速度就越快。并且与基线(第0天)相比,MDR TB治疗显著富集了微生物组中的抗生素抗性基因(ARGs)。
MDR TB治疗期间微生物组恢复的特点是——共生菌的进化
研究人员观察到MDR TB治疗后,患者的微生物组会恢复如初,其主要特征是梭菌目(Clostridiales)的恢复。通过分析患者治疗前后的Klebsiella 和E. coli宏基因组,他们发现治疗前和治疗中的Klebsiella 和E. coli与基线相比存在显著的突变(SNP分析),包括多种膜转运蛋白,如lsrA、mntB等。对治疗前存在但是治疗后迅速降低再恢复的弹性细菌,如Clostridia,显示出显著更高的SNP多样性。
研究数据有力地表明,对抗TB药物并引发细菌耐药性突变的关键是细菌恢复力。为了确定宏基因组种内多样性分析(MIDAS)发现的药物靶点突变是否普遍存在于微生物组中,研究人员使用了对单核苷酸变异具有更高灵敏度的inStrain,检测到诸如 ATP 合成酶ε链和 glpK 中的许多变异。这些数据提供了强有力的证据,即所使用抗生素的耐药性突变在患者中会发生广泛的进化,这也表明,抗生素耐药共生菌和病原菌的选择可能会影响长期抗生素治疗过程中微生物组的动态变化,而且最终,微生物组的恢复力可能是由于共生菌竞争而导致的,即耐药性病原菌被更适合和更耐药的共生菌群代替。
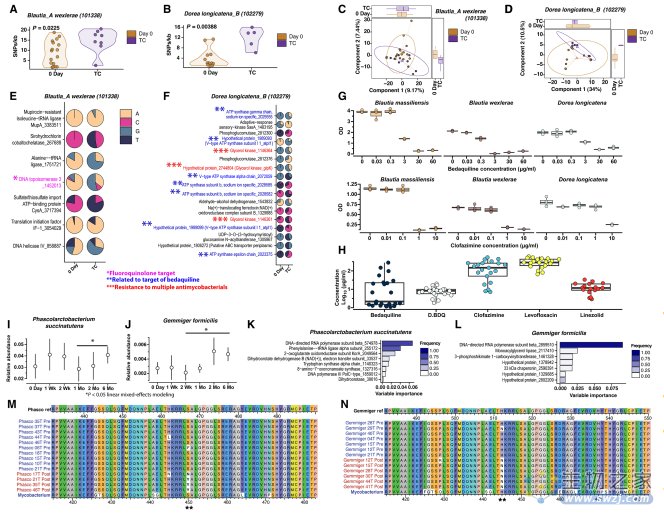
图3. 微生物群恢复力与共生菌出现抗菌药耐药性相对应
治疗 TB 感染是人类持续接触抗生素时间最长的治疗之一。研究结果证实,无论是在疾病还是健康状态下,微生物组的组成都会对全身炎症的动态基调产生重大影响,诸如Clostridia的高丰度会诱导抗炎状态,而Enterobacteriaceae的大量繁殖则会引发炎症加重等。
因此,微生物菌群的相对稳定,对于人体健康而言是至关重要的,并且,研究人员发现在持续的抗生素压力下,共生菌对长期微生物组动态平衡具有巨大的贡献,这意味着共生菌具有潜在超越病原菌的内在能力,如果其能够在抗生素的选择性压力下进化,那么它们就有能力超越病原菌及其编码的 ARGs。
参考文献:
1. Shakti K. Bhattarai et al. ,Commensal antimicrobial resistance mediates microbiome resilience to antibiotic disruption. Sci. Transl. Med.16,eadi9711(2024)































