2023年4月18日,Palleon Pharmaceuticals 在美国癌症研究协会(AACR)2023年年会上公布了其在研疗法E-602的1期临床试验结果,这些数据证明了其全球首创的糖免疫检查点抑制剂的作用机制及剂量依赖性降低免疫细胞表面唾液酸化修饰并激活免疫系统,此外该疗法耐受性良好,无剂量限制毒性,这些结果支持将E-602推进到2期临床阶段。
Palleon 公司由2022年诺贝尔化学奖得主、生物正交化学开创者 Carolyn Bertozzi 教授创立,Palleon 公司的EAGLE(酶-抗体聚糖配体编辑)平台正是基于 Carolyn Bertozzi 教授的研究成果。

Carolyn Bertozzi 教授
真正的全球首创
Palleon 公司表示,E-602代表了一种真正的新型免疫肿瘤学候选药物,它建立在糖生物学的基础上,糖生物学为癌症和其他疾病的药物开发提供了前所未有的机会。这些初步临床数据为启动进一步的2期临床试验提供了必要的验证。

Carolyn Bertozzi 教授表示,看到EAGLE平台开发的候选药物的首个临床结果令人兴奋,Palleon正在推进一种由唾液酸聚糖(sialoglycan)及其受体之间的相互作用定义的全新免疫调节轴,这可能使对当前药物无反应的患者受益。
Carolyn Bertozzi 教授在之前的研究中发现,肿瘤细胞和免疫细胞表面的高唾液酸化(Hypersialylation)是癌症免疫逃逸的重要原因。
唾液酸聚糖(Sialoglycan)介导的免疫抑制涉及超过12个抑制性免疫检查点受体,每一个都可以结合许多不同的唾液酸聚糖。传统的药物开发是以一对一的结合关系为目标,而这并不适用于唾液酸聚糖及其受体之间的免疫调节轴,因为这一调节轴有太多冗余,无法有效地靶向单个受体或配体。
Palleon 的研究人员发现了唾液酸聚糖介导的免疫逃逸的致命弱点——所有阻断免疫系统杀伤作用的Siglec受体都依赖于唾液酸的存在。因此,如果能从肿瘤细胞和免疫细胞表面去除唾液酸化,就有望激活免疫系统,实现全面抗肿瘤免疫反应。
E-602是工程化人唾液酸酶与人IgG1 Fc区融合蛋白,这是一款双功能唾液酸酶融合蛋白,通过唾液酸酶降解高唾液酸化的肿瘤细胞和免疫细胞上的免疫抑制性唾液酸聚糖,从而恢复机体的抗肿瘤免疫反应。
E602作用原理
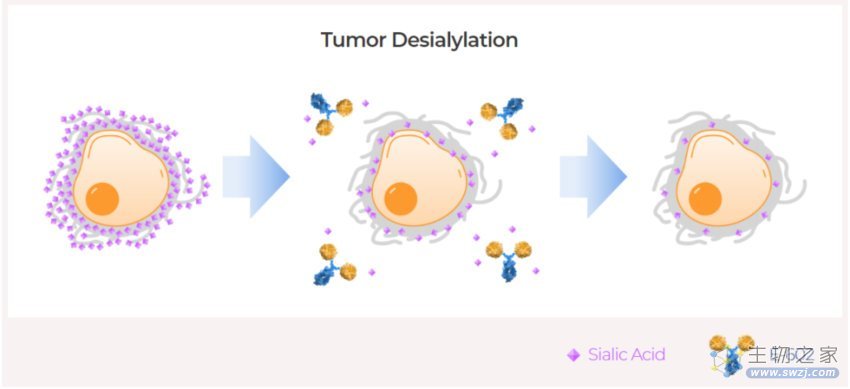
E602去除肿瘤细胞唾液酸化
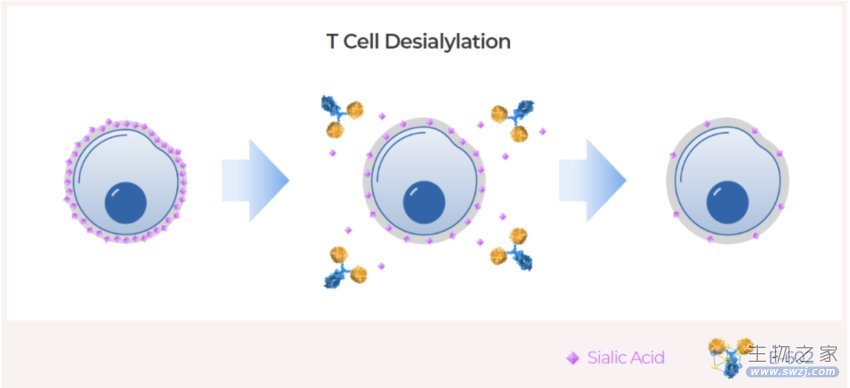
E602去除T细胞唾液酸化
E602临床试验数据
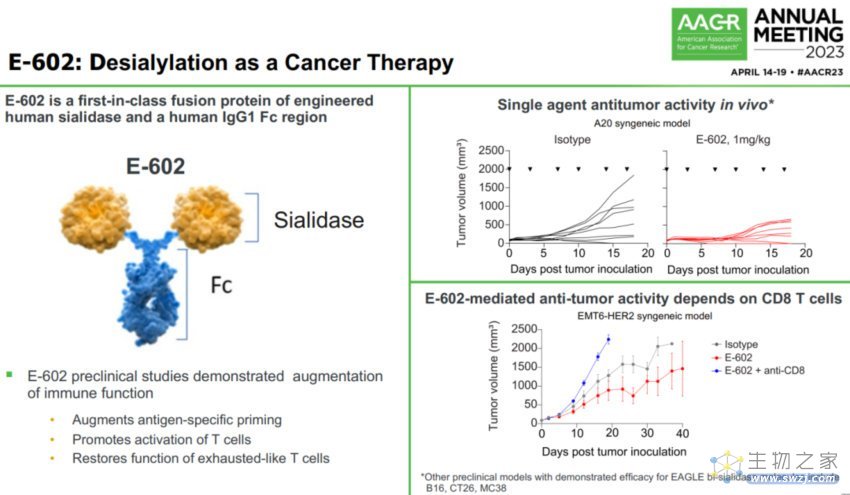
E602:基于去唾液酸化的癌症疗法
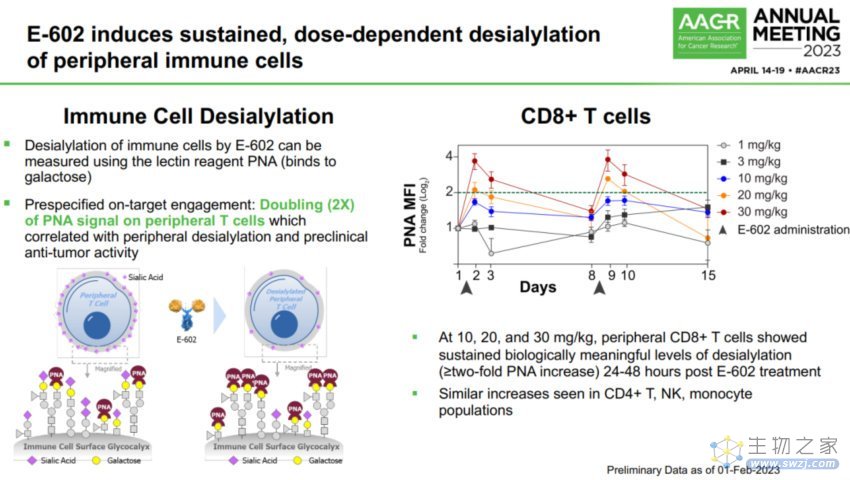
E-602诱导持续的、剂量依赖性的外周免疫细胞去唾液酸化
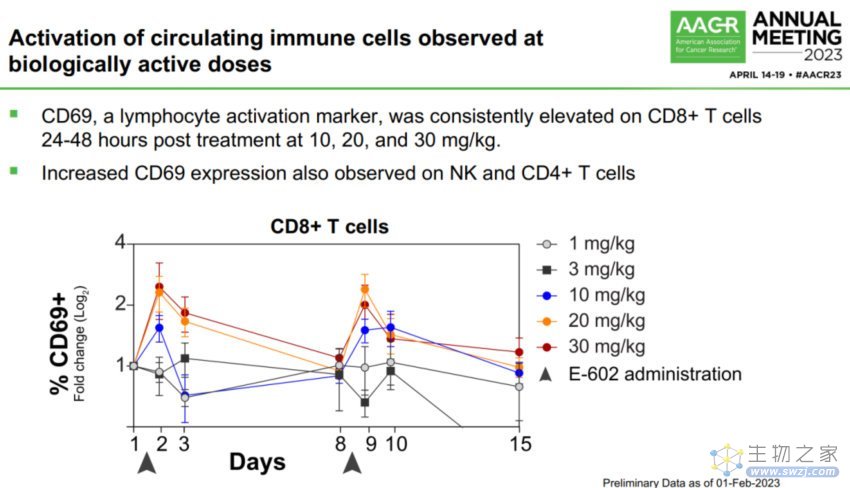
E602激活循环免疫细胞
具体来说,40名癌症患者接受了至少一剂E-602的治疗,包括21名结直肠癌患者和10名胰腺癌患者,耐受剂量高达30mg/kg,且无剂量限制毒性。通过循环中活化免疫细胞的增加和循环细胞因子和趋化因子的升高,观察到剂量依赖性的去唾液酸化和免疫系统激活。据悉,2期临床试验还将评估E-602单药治疗肺癌和黑色素瘤患者的临床活性。
开创生物正交化学
Carolyn Bertozzi 1988年本科毕业于哈佛大学,此后,她在加州大学伯克利分校读博,三年级时,她的导师因患上了直肠癌,无法给予正常的研究指导,一年后她的导师离开加州大学伯克利分校前往斯坦福大学。在这种情况下,Carolyn Bertozzi 开始自我指导做实验、写论文、申请基金,在四年级时她发表了6篇第一作者论文,并于1993年顺利博士毕业,博士毕业后,她申请到了美国癌症协会的博士后奖学金,从化学领域进入生物学领域。1996年,Carolyn Bertozzi 加入加州大学伯克利分校任助理教授,1999年升任副教授,2002年成为教授,2003年当选美国艺术与科学学院院士(AAAS),2005年当选美国国家科学院院士(NAS)。2015年,她加入了斯坦福大学,并任职至今。
2001年,K. Barry Sharpless、Morten Meldal 等人报道了由铜离子催化的叠氮基团和末端炔基之间发生的点击化学反应(click reaction),此后,许多实验室开始使用这个高效反应进行生物分子标记和研究。但是铜离子本身的毒性,导致点击化学在细胞和活体内的应用受到很大限制。
2003年,Carolyn Bertozzi 提出了生物正交化学 (Bioorthogonal Chemistry),能够在生物体内复杂的环境下,让外源分子或官能团快速高效地发生反应,同时又不影响生物体内分子间正常反应。在她的努力下,点击化学进入了一个新的层面,实现了无铜化,因此能够在生物体内安全应用。
2022年10月5日,美国斯坦福大学的 Carolyn Bertozzi、丹麦哥本哈根大学的 Morten Meldal、美国斯克里普斯研究所的 K. Barry Sharpless 三人荣获2022年诺贝尔化学奖。三人因对点击化学和生物正交化学发展做出的贡献而获奖。Barry 和 Morten 为点击化学奠定了基础,而 Carolyn 则将点击化学带到了一个新的层面,并开始在生物体内利用它。
从实验室到临床治疗
Carolyn Bertozzi 实验室利用生物正交反应来追踪生物体内的分子间相互作用,以及它们对疾病的作用,并对细胞、组织、器官进行标记和成像。他们还发现,肿瘤细胞表面的聚糖可以保护肿瘤细胞免受免疫系统的杀伤作用。基于这些发现,他们开发了一种全新的抗癌药物类型,将分解聚糖的唾液酸酶与肿瘤特异性抗体结合,增强癌症治疗效果。
基于上述发现,Carolyn Bertozzi 于2015年创立了 Palleon Pharmaceuticals 公司,致力于开发糖介导的免疫调节治疗癌症和炎症性疾病,例如将唾液酸酶与PD-L1或HER2抗体形成融合蛋白,实现双管齐下的抗癌效果。其靶向肿瘤细胞和免疫细胞上的免疫抑制性唾液聚糖的双功能唾液酸酶融合蛋白药物E-602正在进行1/2期临床试验。
目前,Palleon 共有4条肿瘤研发管线,其中进度最快的是E-602,处于1/2期临床试验阶段。这是基于 Palleon 公司的EAGLE(酶-抗体聚糖配体编辑)平台开发的第一个工程化人类基因融合蛋白,这是一款双功能唾液酸酶融合蛋白,通过酶促反应去除肿瘤细胞和免疫细胞表面的唾液酸聚糖,解除其诱导的免疫抑制作用,从而增强抗肿瘤免疫能力。
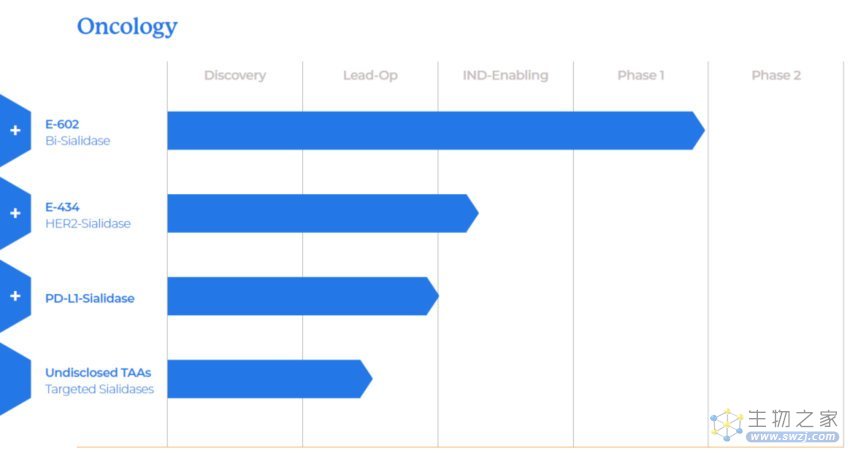
其余三条管线分别是双功能抗PD-L1抗体-唾液酸酶融合蛋白,双功能抗HER2抗体-唾液酸酶融合蛋白,以及一款未公开靶点的肿瘤相关抗原-唾液酸酶融合蛋白。后两条管线与复宏汉霖合作开发。此外,Palleon 还有三款针对炎症疾病的研发管线,目前均处于临床前阶段。
参考资料:
https://palleonpharma.com/news/
https://palleonpharma.com/wp-content/uploads/AACR2023_Palleon-04172023-for-Website.pdf































