在合成生物学中,人们总是希望将细菌基因组改造出有益性状。当使用这些改造的细菌来发酵生产药物(例如胰岛素)或其他有用物质(例如生物燃料)时,有两个需要警惕两方面的问题。一方面是,如果这些发酵罐中的细菌被病毒污染,就会导致生产中断,造成巨大损失。另一方面是,需要防止这些改造过的细菌逃逸到自然界,造成潜在危害。
此前已有一些研究通过对生物体进行密码子工程设计,以防止病毒感染和基因的水平转移,从而为自然生态系统建立“防火墙”。然而,许多病毒和可移动遗传元件自带的部分翻译装置,可能使得“防火墙”失效。
2023年3月15日,哈佛大学乔治·丘奇(George Church)实验室在 Nature 发表了题为:A swapped genetic code prevents viral infections and gene transfer 的研究论文。
该研究在基因工程和合成生物学领域迈出了一大步,创造出了一种可以抵抗迄今已知所有天然病毒感染的大肠杆菌。而且,研究团队还在这种改造的大肠杆菌中加了双保险,能最大程度上防止这种改造的大肠杆菌及其修饰基因逃逸到自然界。
这项研究能够在利用合成生物学技术生产药物或其他有用物质时避免病毒污染带来的巨大损失。而且,该技术还可以用用于转基因生物中,能够防止转基因的逃逸及其可能带来的潜在危害。
值得一提的是,论文作者还包括来自金斯瑞生物(GenScript)的三位员工。

论文第一作者 Akos Nyerges 表示,我们首次开发出了一种技术来设计一种不会被任何已知病毒感染的生物体,截至目前,广泛的实验室研究和计算分析显示,还没有一种病毒能够感染它们。而且,我们还在其基因组中内置了安全措施,以防止这些被修改过的遗传物质进入自然界中。
2022年10月,剑桥大学的研究人员在 Science 期刊发表了一篇题为:Refactored genetic codes enable bidirectional genetic isolation 的研究论文。该研究团队认为,他们通过重构遗传密码开发出了一种对病毒免疫的大肠杆菌——Syn61Δ3。
剑桥大学团队所使用的的方法是对大肠杆菌基因组进行重组,使其从61组密码子中编码维持生命所需的全部蛋白质,而不是自然状态下的64组密码子。按照这一设想,病毒难以在缺失了几组密码子的大肠杆菌内复制,也就无法感染和劫持细胞。

然而,Akos Nyerges 等人对大肠杆菌流行的地方进行采样,例如鸡舍、鼠窝、污水,从中发现了可以感染上述改造的大肠杆菌的病毒。也就是说,这种改造的大肠杆菌并不能完全抵御病毒感染。他们发现,仅仅减少几组密码子是不够的,有些病毒能够绕过这些缺失的密码子。
乔治·丘奇团队认为,要想构建出真正抵抗任何病毒感染的生物体,关键在于转运RNA,也就是tRNA。

乔治·丘奇
我们知道,mRNA上每三个碱基组成一个密码子,对应一个氨基酸,在mRNA翻译成蛋白质的过程中,tRNA通过自身的反密码子识别mRNA上的密码子,并将该密码子对应的氨基酸转运至核糖体合成的多肽链上,从而执行mRNA翻译蛋白质的过程。

在mRNA翻译蛋白质过程中,六种密码子均对应着丝氨酸,剑桥大学团队删除了其中两个丝氨酸密码子TCG和TCA,以及对应的tRNA。乔治·丘奇团队进一步添加了新的诱骗tRNA,这些诱骗tRNA会把TCG和TCA从原本的丝氨酸识别为亮氨酸。
而亮氨酸和丝氨酸在物理和化学上的区别是最大的。当入侵病毒(噬菌体)注入自己充满TCG和TCA的遗传密码,并尝试劫持大肠杆菌制造病毒蛋白时,这些tRNA就会打乱病毒的合成指令,在蛋白质序列中引入错误的氨基酸,从而合成无功能的病毒蛋白质,这也意味着病毒无法完成复制,也就无法进一步感染更多细胞。
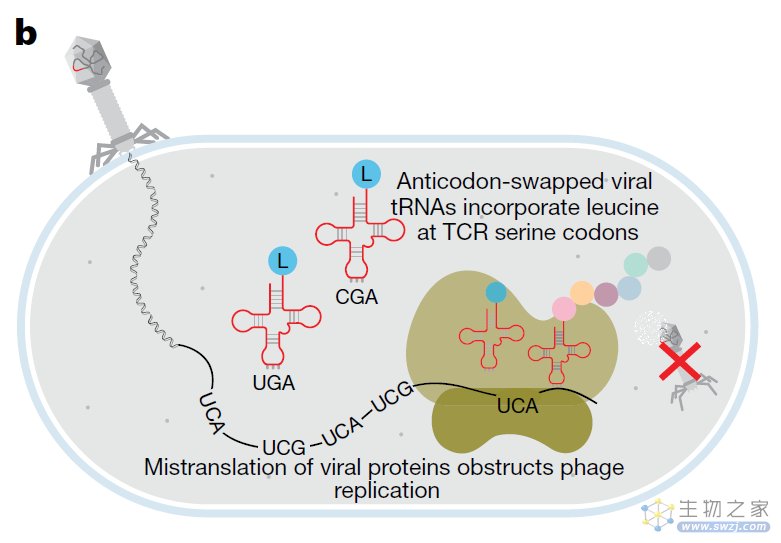
病毒蛋白的错误翻译阻碍了病毒的复制
虽然病毒也配备了自己的tRNA,它们能够将TCG和TCA正确转换为丝氨酸,但研究团队证实,在大肠杆菌中引入的诱骗tRNA效率很高,能够压倒来自病毒的tRNA。
研究团队表示,这项工作可能已经清除了使细菌对所有病毒免疫的最后一个障碍,构建出了对已知病毒完全免疫的生物体,如果病毒想要突破这一点,就需要同时产生几十种特定的突变,这对自然进化来说,非常非常不可能出现。
为了保险起见,研究团队还在改造的大肠杆菌上添加了两个独立的保障措施。
第一个保障措施是防止水平基因转移,这是一种不断发生的自然现象,指遗传物质被水平转移给非子代的其他细胞。由于研究团队在改造的大肠杆菌中将亮氨酸的密码子替换成了TCG或TCA,如果这些改造的大肠杆菌的遗传物质水平转移到了其他生物体中,那么这些生物体的天然tRNA仍然将TCG和TCA转换为丝氨酸,从而得到一堆没有进化优势的乱码蛋白。同样,如果改造的大肠杆菌的诱骗tRNA被水平转移到了其他生物体,那么这些诱骗tRNA会将代表丝氨酸的密码子误读为亮氨酸密码子,从而杀死细胞,防止进一步传播。
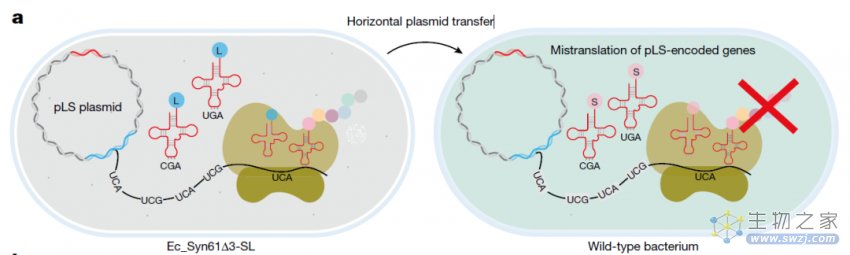
TCG或TCA编码亮氨酸,抑制了水平基因转移
也就是说,任何逃逸的诱骗tRNA都“走不远”,因为它们对自然生物体有毒。这也代表了第一种能够阻止转基因生物的基因水平转移到天然生物的技术。
第二个保障措施是,研究团队设计的细菌本身无法在受控环境之外生存。这些改造的大肠杆菌必须依赖实验室制造的非天然氨基酸生存,这种非天然氨基酸在自然界并不存在。因此,它们一旦逃逸,就会因为缺乏非天然氨基酸来源而迅速死亡。因此,不会有人类或者其他生物体被这些大肠杆菌感染的风险。
最后,研究团队表示,希望使用这种改造的大肠杆菌来生产医用合成材料,从而告别之前昂贵的化学合成。合成生物学的大门正在徐徐打开,而新的探索才刚刚开始。
论文链接:
https://www.nature.com/articles/s41586-023-05824-z
https://www.science.org/doi/10.1126/science.add8943































